Этапы дифференцировки клеток иммунной системы
Учебник состоит из семи частей. Часть первая – «Общая микробиология» – содержит сведения о морфологии и физиологии бактерий. Часть вторая посвящена генетике бактерий. В части третьей – «Микрофлора биосферы» – рассматривается микрофлора окружающей среды, ее роль в круговороте веществ в природе, а также микрофлора человека и ее значение. Часть четвертая – «Учение об инфекции» – посвящена патогенным свойствам микроорганизмов, их роли в инфекционном процессе, а также содержит сведения об антибиотиках и механизмах их действия. Часть пятая – «Учение об иммунитете» – содержит современные представления об иммунитете. В шестой части – «Вирусы и вызываемые ими заболевания» – представлены сведения об основных биологических свойствах вирусов и о тех заболеваниях, которые они вызывают. Часть седьмая – «Частная медицинская микробиология» – содержит сведения о морфологии, физиологии, патогенных свойствах возбудителей многих инфекционных заболеваний, а также о современных методах их диагностики, специфической профилактики и терапии.
Учебник предназначен для студентов, аспирантов и преподавателей высших медицинских учебных заведений, университетов, микробиологов всех специальностей и практических врачей.
5-е издание, исправленное и дополненное
Книга: Медицинская микробиология, иммунология и вирусология
Происхождение и дифференцировка клеток иммунной системы
Происхождение и дифференцировка клеток иммунной системы
Не все индуцированные антигеном В-лимфоциты подвергаются дифференцировке до конца. Часть из них после нескольких циклов деления перестает размножаться и образует субклон клеток памяти (из одной В-клетки образуется около 1000 клеток памяти, таким же образом образуются клетки памяти и из Т-лимфоцитов). Клетки памяти определяют продолжительность приобретенного иммунитета. При повторном контакте с данным антигеном они быстро превращаются в клетки-эффекторы. При этом В-клетки памяти обеспечивают синтез антител в более короткие сроки, в большем количестве и с более высоким сродством антител другого класса иммуноглобулинов – IgG вместо IgM. Эта перестройка происходит благодаря рекомбинации генов Н-цепи: тандем генов V ? D ? J переносится с С?-гена к одному из СН-генов – ?, ?, ?. Ее вызывает сигнал, получаемый СD40-рецептором В-клеток памяти, когда они выходят из зародышевого центра в пул памяти, от gp39-рецептора Т-хелперов. Установлено, что мутации в гене, кодирующем gp39, являются причиной редкого тяжелого первичного иммунодефицита – гипер-IgM-синдрома. Отсутствие у Т-хелперов молекул gp39 в этих случаях приводит к утрате ими способности связываться с CD40, что ведет к неправильному ответу на Т-зависимый антиген – гиперпродукции IgM.
В ходе антигензависимой дифференцировки В-лимфоцитов используется и механизм соматических мутаций в V-генах. Они происходят с частотой в 10 000 раз большей частоты спонтанных мутаций и ограничиваются определенной стадией дифференцировки, а именно – периодом перехода от продукции IgM к продукции IgG. Благодаря этим мутациям обеспечивается максимальная подгонка структуры активного центра антитела к детерминанту антигена.
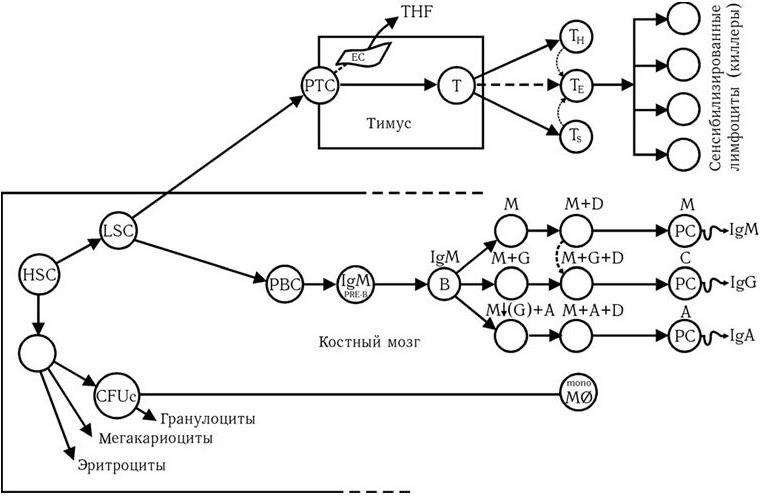
Таким образом, наиболее важными событиями дифференцировки В-лимфоцитов являются: 1) сборка гена иммуноглобулина из его фрагментов, содержащихся в ДНК эмбриональных клеток; 2) формирование пула клеток памяти; 3) возникновение новых вариантов генов Ig в результате дополнительных класс-переключающих рекомбинаций; 4) вспышка соматических мутаций на строго определенной стадии дифференцировки. В результате этих событий происходит образование множества генетически стабильных клонов антителообразующих клеток (вероятно, не менее чем 10 8 ). Общая схема происхождения и дифференцировки Т– и В-лимфоцитов и макрофагов из исходных стволовых клеток представлена на рис. 71.
В соответствии с этой схемой, исходная костно-мозговая клетка (HSC) генерирует два типа предшественников: лимфоидную стволовую клетку (LSC), от которой происходят клетки-предшественники Т-лимфоцитов (PTC), клетки-предшественники В-лимфоцитов (PBC); и клетку, являющуюся предшественником клеток красной крови, от которой, в свою очередь, происходит предшественник лейкоцитов (CFUc) и берет начало система мононуклеарных макрофагов. Предшественники Т-лимфоцитов под влиянием тимуса превращаются в Т-лимфоциты и их субклассы. Пути дифференцировки В-лимфоцитов описаны выше.
В целом система В-лимфоцитов обеспечивает синтез антител, отвечает за иммунитет против большинства бактериальных и вирусных инфекций, анафилаксию и другие реакции гиперчувствительности немедленного типа, некоторые аутоиммунные болезни, за формирование клеток иммунной памяти и иммунологическую толерантность.
Система T-лимфоцитов играет регуляторную роль по отношению к B-лимфоцитам, отвечает за все реакции гиперчувствительности замедленного типа, иммунитет против вирусных и некоторых бактериальных инфекций (туберкулез, бруцеллез, туляремия и др.), осуществляет иммунологический надзор, отвечает за противоопухолевый иммунитет, иммунологическую толерантность, некоторые виды иммунопатологии.
Рис. 71. Схема происхождения и дифференцировки клеток-эффекторов иммунной системы (ВОЗ, 1978).
источник
Этапы дифференцировки клеток иммунной системы
B-лимфоциты (B-клетки, от bursa fabricii птиц, где впервые были обнаружены) — функциональный тип лимфоцитов, играющих важную роль в обеспечении гуморального иммунитета. При контакте с антигеном или стимуляции со стороны T-клеток некоторые B-лимфоциты трансформируются в плазматические клетки, способные к продукции антител. Другие активированные B-лимфоциты превращаются в B-клетки памяти. Помимо продукции антител, В-клетки выполняют множество других функций: выступают в качестве антигенпрезентирующих клеток, продуцируют цитокины и экзосомы.
У эмбрионов человека и других млекопитающих B-лимфоциты образуются в печени и костном мозге из стволовых клеток, а у взрослых млекопитающих — только в костном мозге. Дифференцировка В-лимфоцитов проходит в несколько этапов, каждый из которых характеризуется присутствием определённых белковых маркеров и степенью генетической перестройки генов иммуноглобулинов.
Аномальная активность В-лимфоцитов может быть причиной аутоиммунных и аллергических заболеваний.
Существует несколько подтипов В- лимфоцитов. Основная функция В- клеток— эффекторное участие в гуморальных иммунных реакциях, дифференциация в результате антигенной стимуляции в плазматические клетки, продуцирующие антитела. Развитие В-лимфоцитов в течение всего постэмбрионального периода протекает в костном мозге. Под воздействием клеточного костномозгового микроокружения и гуморальных факторов костного мозга из стволовой лимфоидной клетки формируются В-лимфоциты. Ранние этапы развития В-лимфоцитов зависят от прямого контактного взаимодействия со стромальными элементами. Более поздние этапы развития В-лимфоцитов протекают под воздействием гуморальных факторов костного мозга.
Образование В- клеток у плода происходит в печени, в дальнейшем- в костном мозге. Процесс созревания В- клеток осуществляется в две стадии:
- антиген- независимую,
- антиген — зависимую.
Антиген -независимая фаза. В- лимфоцит в процессе созревания проходит стадию пре-В- лимфоцита- активно пролиферирующей клетки, имеющей цитоплазменные H- цепи типа C мю (т.е. IgM). Следующая стадия- незрелый В- лимфоцит характеризуется появлением мембранного (рецепторного) IgM на поверхности. Конечная стадия антигеннезависимой дифференцировки- образование зрелого В- лимфоцита, который может иметь два мембранных рецептора с одинаковой антигенной специфичностью (изотипа) — IgM и IgD. Зрелые В- лимфоциты покидают костный мозг и заселяют селезенку, лимфоузлы и другие скопления лимфоидной ткани, где их развитие задерживается до встречи со “своим” антигеном, т.е. до осуществления антиген- зависимой дифференцировки.
Антиген- зависимая дифференцировка включает:
- активацию,
- пролиферацию,
- дифференцировку В- клеток в плазматические клетки и В- клетки памяти.
Активация осуществляется различными путями, что зависит от свойств антигенов и участия других клеток ( макрофагов, Т- хелперов). Большинство антигенов, индуцирующих синтез антител, для индукции иммунного ответа требуют участия Т- клеток- тимус- зависимые антигены. Тимус- независимые антигены (ЛПС, высокомолекулярные синтетические полимеры) способны стимулировать синтез антител без помощи Т- лимфоцитов.
В- лимфоцит с помощью своих иммуноглобулиновых рецепторов распознает и связывает антиген. Одновременно с В- клеткой антиген по представлению макрофага распознается Т- хелпером (Т- хелпером 2), который активируется и начинает синтезировать факторы роста и дифференцировки. Активированный этими факторами В- лимфоцит претерпевает ряд делений и одновременно дифференцируется в плазматические клетки, продуцирующие антитела.
Пути активации В- клеток и кооперации клеток в иммунном ответе на различные антигены и с участием популяций, имеющих и не имеющих антиген Lyb5 популяций В- клеток отличаются. Активация В- лимфоцитов может осуществляться:
- Т- зависимым антигеном при участии белков МНС класса 2 Т- хелпера;
- Т- независимым антигеном, имеющим в составе митогенные компоненты;
- поликлональным активатором (ЛПС);
- анти- мю иммуноглобулинами;
Т- независимым антигеном, не имеющим митогенного компонента.
источник
Тема 12. ИММУНОЦИТОПОЭЗ И УЧАСТИЕ ИММУННЫХ КЛЕТОК РЕАКЦИЯХ ИММУНИТЕТА
Тема 12. ИММУНОЦИТОПОЭЗ И УЧАСТИЕ ИММУННЫХ КЛЕТОК РЕАКЦИЯХ ИММУНИТЕТА
В отличие от миелопоэза лимфоцитопоэз в эмбриональном и постэмбриональном периодах осуществляется поэтапно, сменяя разные лимфоидные органы. Как отмечалось ранее, лимфоцитопоэз подразделяется на:
В свою очередь, они делятся на три этапа:
2) этап антигеннезависимой дифференцировки, осуществляемый в центральных иммунных органах;
3) этап антигензависимой дифференцировки, осуществляемый в периферических лимфоидных органах.
Т-лимфоцитопоэз
Первый этап осуществляется в лимфоидной ткани красного костного мозга, где образуются следующие классы клеток:
1) стволовые клетки – I класс;
2) полустволовые клетки предшественники Т-лимфоцитопоэза – II класс;
3) унипотентные Т-поэтинчувствительные клетки, предшественницы Т-лимфоцитопоэза. Эти клетки мигрируют в кровяное русло и достигают вилочковой железы (тимуса) – III класс.
Второй этап – антигеннезависимая дифференцировка, которая осуществляется в корковом веществе тимуса. При этом происходит дальнейшее образование Т-лимфоцитов. Стромальными клетками выделяется тимозин, под влиянием которого происходит превращение унипотентных клеток в Т-лимфобласты. Они являются клетками IV класса в Т-лимфоцитопоэзе. Т-лимфобласты превращаются в Т-пролимфоциты (клетки V класса), а они в Т-лимфоциты – VI класс.
В тимусе из унипотентных клеток развиваются самостоятельно три субпопуляции Т-лимфоцитов – Т-киллеры, Т-хелперы, Т-супрессоры.
Образовавшиеся Т-лимфоциты приобретают в корковом веществе тимуса разные рецепторы к разнообразным антигенам, при этом сами антигены в тимус не поступают. Защита вилочковой железы от попадания чужеродных антигенов осуществляется за счет наличия гематотимусного барьера и отсутствия приносящих сосудов в тимусе.
В результате второго этапа образуются субпопуляции Т-лимфоцитов, которые обладают различными рецепторами к определенным антигенам. В тимусе также происходит образование Т-лимфоцитов, обладающих рецепторами к антигенам собственных тканей, однако такие клетки сразу же разрушаются макрофагами.
После образования Т-лимфоциты, не проникая в мозговое вещество тимуса, поступают в кровоток и заносятся в периферические лимфоидные органы.
Третий этап (антигеннезависимая дифференцировка) осуществляется в Т-зависимых зонах периферических лимфоидных органов – лимфатических узлах и селезенке. Здесь создаются условия для встречи антигена с Т-лимфоцитом (киллером, хелпером или супрессором), имеющим рецептор к данному антигену.
Чаще всего происходит не непосредственное взаимодействие Т-лимфоцита с антигеном, а опосредованное – через макрофаг. При поступлении в организм чужеродного антигена он вначале фагоцитируется макрофагом (завершенный фагоцитоз), частично расщепляется, а антигенная детерминанта выносится на поверхность макрофага, где концентрируется. Затем эти детерминанты передаются макрофагами на соответствующие рецепторы различных субпопуляций Т-лимфоцитов. Под влиянием специфического антигена происходит реакция бластотрансформации – превращение Т-лимфоцита в Т-лимфобласт. Дальнейшая дифференцировка клеток зависит от того, какая субпопуляция Т-лимфоцитов провзаимодействовала с антигеном.
Т-киллерный лимфобласт дает следующие клоны клеток.
1. Т-киллеры (или цитотоксические лимфоциты), являющиеся эффекторными клетками, обеспечивающими клеточный иммунитет. Т-киллеры обеспечивают первичный иммунный ответ – реакцию организма на первое взаимодействие с антигеном.
В процессе уничтожения киллерами чужеродного антигена можно выделить два основных механизма: контактное взаимодействие – разрушение участка цитолеммы клетки-мишени и дистантное взаимодействие – выделение цитотоксических факторов, действующих на клетку-мишень постепенно и длительно.
2. Клетки Т-памяти. Эти клетки при повторной встрече организма с тем же антигеном обеспечивают вторичный иммунный ответ, который сильнее и быстрее первичного.
Т-хелперный лимфобласт дает следующие клоны клеток:
1) Т-хелперы, секретирующие медиатор лимфокин, стимулирующий гуморальный иммунитет. Это индуктор иммунопоэза;
Т-супрессорный лимфобласт дает следующие клоны клеток:
Таким образом, в ходе третьего этапа Т-лимфоцитопоэза происходит образование эффекторных клеток каждой субпопуляции Т-лимфоцитов (Т-киллеров, Т-хелперов и Т-супрессоров), обладающих определенной функцией, и клеток Т-памяти, обеспечивающих вторичный иммунный ответ.
В клеточном иммунитете можно выделить два механизма уничтожение киллерами клеток-мишеней – контактное взаимодействие, при котором происходит разрушение участка цитолеммы клетки-мишени и ее гибель, и дистантное взаимодействие – выделение цитотоксических факторов, действующих на клетку-мишень постепенно и вызывающих ее гибель через определенное время.
В-лимфоцитопоэз
В процессе В-лимфоцитопоэза можно выделить следующие этапы.
Первый этап – осуществляется в красном костном мозге, где образуются следующие классы клеток:
1) стволовые клетки – I класс;
2) полустволовые клетки, предшественницы лимфопоэза – II класс;
3) унипотентные В-лимфопоэтинчувствительные клетки – предшественницы В-лимфоцитопоэза – III класс.
Второй этап – антигеннезависимая дифференцировка – у птиц осуществляется в специальном органе – фабрициевой сумке, у млекопитающих в том числе и у человек такой орган не найден. Большинство исследователей считает, что второй этап (так же как и первый) осуществляется в красном костном мозге, где образуются В-лимфобласты – клетки IV класса. Затем происходит их пролиферация в В-пролимфоциты – клетки V класса и в В-лимфоциты – клетки VI класса. В процессе второго этапа В-лимфоциты приобретает разнообразные рецепторы к антигенам. При этом установлено, что рецепторы представлены белками – иммуноглобулинами, которые синтезируются в самих же созревающих В-лимфоцитах, затем выносятся на поверхность и встраиваются в плазмолемму. Концевые химические группировки у этих рецепторов различны, и именно этим объясняется специфичность восприятия ими определенных антигенных детерминант разных антигенов.
Третий этап – антигензависимая дифференцировка осуществляется в В-зависимых зонах периферических лимфоидных органов – в селезенке и лимфатических узлах. Тут происходит встреча В-лимфоцитов с антигенами, их последующая активация и трансформация в иммунобласт. Это происходит только при участии дополнительных клеток – макрофагов, Т-хелперов и Т-супрессоров. Следовательно, для активации В-лимфоцитов необходима кооперация следующих клеток – В-лимфоцита, Т-хелпера или Т-супрессора, а также гуморального антигена – бактерии, вируса или белка полисахарида. Процесс взаимодействия протекает следующим образом: антигенпредставляющий макрофаг фагоцитирует антиген и выносит на поверхность клеточной мембраны антигенную детерминанту, после этого детерминанта воздействует на В-лимфоциты, Т-хелперы и Т-супрессоры. Таким образом, влияния антигенной детерминанты на В-лимфоцит недостаточно для реакции бластотрансформации, она протекает после активации Т-хелпера и выделения им активирующего лимфокина. После этого В-лимфоцит превращается в иммунобласт. После пролиферации иммунобласта образуются клоны клеток – плазмоциты – эффекторные клетки гуморального иммунитета, они синтезируют и выделяют в кровь иммуноглобулины – антитела различных классов и клетки В-памяти.
Иммуноглобулины (антитела) взаимодействуют со специфическими антигенами, образуется комплекс «антиген – антитело», таким образом происходит нейтрализация чужеродных антигенов.
Т-хелперы играют следующую функцию в осуществлении гуморального иммунитета – способствуют реакции бластотрансформации, заменяют синтез неспецифических иммуноглобулинов на специфические, стимулируют синтез и выделение иммуноглобулинов плазмоцитами.
Т-супрессоры активируются этими же антигенами и выделяют лимфокины, угнетающие образование плазмоцитов и синтез ими иммуноглобулинов вплоть до полного прекращения. Таким образом, воздействие на В-лимфоцит Т-киллеров и Т-хелперов регулирует реакции гуморального иммунитета.
источник
Биология В-лимфоцита в иммунологии
У В-лимфоцитов создается огромное количество вариантов антигенной специфичности. Именно этой вариабельностью объясняется одна из основных характеристик адаптивного иммунного ответа, — разнообразие, т.е. способность реагировать на разные антигенные детерминанты — эпитопы, даже если индивидуум никогда прежде не встречался с ними.
Среди других важных характеристик адаптивного иммунного ответа можно назвать следующие:
- специфичность — способность различать эпитопы;
- память — способность вспоминать предыдущий контакт с определенным антигеном таким образом, что повторный контакт ведет к развитию более быстрого и эффективного иммунного ответа, чем первичный;
- различение «своего» и «чужого» — способность реагировать на антигены, которые являются «чужими» или «не своими», чтобы избежать реакций на собственные, принадлежащие организму, антигены.
Рассматриваются основные этапы развития В-клетки и то, каким образом она приобретает свои характерные черты, связанные с адаптивным иммунным ответом: разнообразие, специфичность, память и способность к распознаванию «своего» и «чужого».
Места ранней дифференцировки В-клеток
Пониманию процесса дифференцировки В-клеток способствовали исследования на животных, в которых была возможность манипулировать их эмбриональным развитием. По этой причине особенно хорошо изучена дифференцировка В-клеток у цыплят и млекопитающих.
Многие этапы процесса дифференцировки В-клеток являются общими для людей, цыплят и мышей.
Название «В-лимфоциты» появилось во время первых опытов с птицами: было показано, что для синтеза антитела необходим орган, называемый фабрициевой сумкой (карман из эпителия клоаки).
Хирургическое удаление фабрициевой сумки предотвращало синтез антител. Поэтому клетки, превращающиеся в зрелые антителопродуцирующие клетки, стали называться бурсазависимыми или В-клетками.
В отличие от птиц у млекопитающих такой фабрициевой сумки нет, а дифференцировка В-клеток происходит в некоторых определенных участках.
Предшественники В-клеточной линии обнаруживаются на ранних стадиях развития плода в ряде мест, в том числе печени. Позднее по мере развития плода и в течение всей дальнейшей жизни основным лимфоидным органом в котором происходит дифференцировка В-клеток, является костный мозг. В связи с этим костный мозг рассматривается как первичный лимфоидный орган, в котором дифференцируются В-лимфоциты у человека и других млекопитающих.
Онтогенез В-лимфоцитов
Начальные фазы дифференцировки В-клеток: про- и пре-В-клетки.
На рис. 7.1 показаны основные стадии процесса дифференцировки В-клеток. Многие из них определяются специфическими реаранжировками генов lg.

Рис. 7.1. Путь дифференцировки В-лимфоцитов. Пунктирными линиями на пре-В-клетке показаны суррогатные легкие цепи. Две сплошные линии ассоциированные с тяжелой цепью поверхности клетки, представляют сигнальные молекулы Igα и Igβ
В-лимфоциты возникают из гемопоэтических стволовых клеток. Адгезивные взаимодействия со стромой костного мозга, нелимфоидными клетками, формирующими каркас, или матрицу, для костного мозга, а также действие цитокина IL-7 обеспечивают поступление сигналов, способствующих выживанию и усиливающих пролиферацию клеток В-линии на ранних стадиях.
Самой первой из определяемых клеток В-линии является так называемая про-В-клетка, у которой сегмент DH-генa тяжелой цепи реаранжируется к сегменту JH-генa. На следующей стадии пре-В-клетки сегменты VH-гена тяжелой цепи реаранжируются, чтобы соединиться с реаранжированными DHJH-сегментами, сформировав VDJ-структуру. После реаранжировки VDJ размещается рядом с Сμ, и пре-В-клетка синтезирует μ-цепь.
Реаранжировки гена Ig во время этих ранних фаз дифференцировки В-клеток происходят в заданном порядке. Первоначальные реаранжировки D—J в про-В-клетках происходили на обеих хромосомах в локусах Н-цепи одновременно. Хромосома, на которой происходит продуктивная DJ-реаранжировка, далее реаранжирует V-генный сегмент к DJ-структуре. Если эти реаранжировки продуктивны, хромосома производит μ-цепь, а на другой хромосоме прекращается реаранжировка в локусе Н-цепи. Если V—DJ-реаранжировка не продуктивна на первой хромосоме, она тем не менее происходит на другой хромосоме. Если реаранжировка продуктивна на второй хромосоме, тогда данная хромосома продуцирует μ-цепь. Если ни одна из этих реаранжировок не продуктивна, клетка умирает посредством апоптоза, также называемого программируемой смертью клетки.
Основной чертой пре-В-клетки является то, что она экспрессирует μ-цепь в качестве трансмембранной молекулы на своей поверхности вместе с продуктами двух нереаранжируемых генов, называемых λ5 и V-прe-B; оба функционируют вместе как суррогатные легкие цепи. На рис. 7.2, А показано, что μ-цепь и суррогатные легкие цепи экспрессируются на поверхности пре-В-клетки вместе с двумя трансмембранными молекулами: Iga (CD79a) и Igβ (CD79b), которые тесно связаны друг с другом дисульфидной связью. Комплекс из μ-цепей и суррогатных легких цепей в соединении с Iga и Igβ называют пре-В-клеточным рецептором (пpe-BCR).
Иммуноглобулины α и β ассоциируются с мембранными молекулами Ig на всех клетках В-клеточной линии: от пре-В-клетки до В-клетки памяти (см. рис. 7.1). Комплекс Igα и Igβ, ассоциированный с мембранными молекулами Ig более зрелых клеток В-лимфоцитарной линии, называется В-клеточным рецептором (BCR); он показан на рис. 7.2, Б. Иммуноглобулины α и β не связываются с антигеном. Их функция — передавать сигналы ядру клетки, что ведет к изменению структуры экспрессируемых генов, в связи с чем Igα и Igβ относят к молекулам, передающим сигнал, ассоциированным с пpe-BCR и BCR. Молекулы, передающие сигнал, также ассоциированы с антигенспецифичным рецептором, экспрессируемым на разных стадиях развития Т-лимфоиита.

Рис. 7.2. (А) Пре-В-клеточный рецептор (пре-BCR). (Б) В-клеточный рецептор (BCR). Тяжелой цепью пpe-BCR является μ-цепь; тяжелой цепью BCR может быть μ-, δ-, γ-, α- или ε-цепь. Иммунорецепторная тирозинсодержащая активационная последовательность (мотив) (ITAM), изображена как прямоугольник в полипептидах Igα и Igβ
На зрелых В-клетках роль Igα и Igβ в BCR заключается в передаче сигналов после того, как антиген свяжется с вариабельным доменом поверхностного Ig. Однако свидетельства того, что пpe-BCR связывается с антигеном, отсутствуют. Данные скорее указывают на то, что Igα и Igβ, ассоциированные с пpe-BCR, сообщают клетке, что она успешно реаранжировала гены Н-цепи Ig и создала функциональную μ-цепь. В результате этого сигнала клетка, экспрессирующая пpe-BCR, дифференцируется дальше: пролиферирует, прекращает синтез суррогатных легких цепей, начинает реаранжировку гена L-цепи и прекращает дальнейшую реаранжировку гена Н-цепи.
Реаранжировка легкой цепи в более поздних фазах развития пре-В-клетки также последовательна: гены к-цепи реаранжируются первыми, но если ни одна из хромосом, кодирующих к-цепи, успешно не реаранжируется. происходит реаранжировка λ-гена. (Если не происходит продуктивной реаранжировки L-цепи, клетка погибает.) Биологическим следствием использования генов только одной хромосомы для производства Н- и L-цепи (аллельного исключения) является то, что отдельная В-клетка экспрессирует на своей поверхности молекулу Ig, специфичную только к одному определенному антигену.
Незрелые В-клетки
На следующей стадии дифференцировки В-клеток L-цепи составляют пары с μ-цепями, формируя мономерный IgM, который вставляется в мембрану. Клетка, несущая только мономерный IgM в качестве антигенспецифичного рецептора, относится к незрелым В-клеткам. Первые эксперименты показали, что незрелая В-клетка может распознавать и отвечать на чужеродный антиген, но это взаимодействие приводит скорее к длительной инактивации, чем к клональной пролиферации и дифференцировке.
Более поздние исследования показали, что незрелая В-клетка может взаимодействовать с аутологичными молекулами в костном мозге, что также может привести к ее инактивации. Такое взаимодействие аутологичных молекул и В-клеток играет важную роль в установлении аутотолерантности у клеток В-линии. поскольку предотвращает развитие потенциально аутореактивных клеток.

Рис. 7.3. Взаимодействие незрелой В-клетки с аутоантигенами
На рис. 7.3 показаны два варианта развития аутотолерантности. Если незрелая В-клетка встречается с собственной молекулой, экспрессируемой на поверхности клеток костного мозга, она погибает посредством апоптоза (делеция). Напротив, если незрелая В-клетка встречается с молекулой, не находящейся на поверхности клетки (растворимый антиген) в костном мозге, она инактивируется, но не устраняется, а, как говорится, становится анергичной. Инактивацию незрелых В-клеток, обладающих потенциальной аутореактивностью при взаимодействии с аутологичными молекулами, называют негативной селекцией. Развивающиеся Т-лимфоциты также проходят через негативную селекцию в процессе дифференцировки в тимусе.
На рис. 7.3 также изображен и третий возможный исход взаимодействия незрелой В-клетки с аутологичной молекулой, а именно реактивация клеточной V(D)J-рекомбиназы — феномен, известный как редактирование рецептора. Вследствие этого гены L-цепи Ig проходят вторичную реаранжировку, используя переаранжированные V- и J-элементы. Например, в показанной на рис. 6.3 клетке, реаранжирующей свой к-локус, V1 и J5 являются переаранжированными генами, которые могут быть использованы для повторной реаранжировки. Редактирование рецептора может привести к появлению специфичности к «чужому» антигену, и незрелая клетка таким образом «спасется» от инактивации.
Зрелые В-клетки
Синтез антител и переключение класса
Взаимодействие антигена со зрелой IgM+IgD+-B-клеткой обычно приводит к активации в отличие от описанной ранее инактивации при взаимодействии антигена с незрелой IgМ+-В-клеткой. В основном они взаимодействуют во вторичных лимфоидных органах, лимфатических узлах и селезенке. Большинство антигенов, особенно белки, называют тимусзависимыми, поскольку для того чтобы В-клетки синтезировали антитела, необходимы хелперные Т-клетки. Первоначальное взаимодействие антигена, хелперных Т-клеток и зрелых В-лимфоцитов осуществляется на границе В- и Т-зависимых областей вторичного лимфоидного органа.
В-клетки увеличиваются (и называются теперь В-клеточными бластами) и пролиферируют. Некоторые из активированных В-клеток могут дифференцироваться далее в специализированную конечную стадию — плазматические клетки, которые способны синтезировать и секретировать антитела (показано справа на рис. 7.1). Антитела, секретируемые отдельной плазматической клеткой, обладают той же антигенной специфичностью, что и Ig на поверхности В-клетки, которая изначально была активирована антигеном. Плазматические клетки не экспрессируют мембранные формы Ig.
Антитела класса IgM синтезируются на ранних стадиях иммунного ответа. Позднее потомство IgM+IgD+-B-кдеток, которые первоначально реагировали на антиген, может продуцировать антитела разных изотипов. Это переключение класса (изотипа) происходит в результате синтеза цитокинов, вырабатываемых хелперными Т-клетками, и контактного взаимодействия В- и Т-клеток. Соответственно, IgM+IgD+-B-клетки переключаются на синтез молекул IgA, IgG или IgE Какой бы изотип Ig ни продуцировался, все дочерние клетки обладают одинаковой антигенной специфичностью.
Созревание аффинности и формирование клеток памяти
Еще позднее в процессе иммунного ответа на тимусзависимые антигены некоторые из активированных В-клеток формируют во вторичном лимфоидном органе специализированный участок — так называемый зародышевый центр. На рис. 7.4 показано, что зародышевый центр преимущественно состоит из активированных В-клеток, меньшего количества Т-клеток и небольшого числа специализированных клеток, называемых фолликулярными дендритными клетками, которые удерживают антиген на своей поверхности и презентируют его В-клеткам.
На рис. 7.4 показано также, что зародышевый центр является местом интенсивной пролиферации В-клеток. Во время этого значительного увеличения их первоначальной популяции В-клетки с мутациями в вариабельной области генов Ig появляются с гораздо большей частотой, чем обычно. Этот соматический гипермутагенез приводит к появлению В-клеток чьи гены вариабельных областей Ig могут синтезировать антитела с более высокой аффинностью к активирующему антигену, чем был у первоначальной В-клетки, активированной антигеном.
Недавние наблюдения дают основания полагать, что гипермутагенез возникает в результате действия фермента, индуцируемого при активации В-клеток. В гене V-области Ig фермент превращает цитозин в урацил; попытки исправить это «неправильное основание» с помощью «механизмов восстановления» в клетке часто приводят к ошибкам и появлению мутаций.

Рис. 7.4. Развитие В-клеток в зародышевом центре: соматический гипермутагенез, созревание аффинности и формирование В-клеток памяти
В-клетки, у которых повышена аффинность генов V-области, селектируются для создания клона и размножаются в зародышевом центре, в то время как В-клетки без мутаций в V-областях не проходят селекцию и погибают. Таким образом, соматический гипермутагенез приводит к увеличению продукции антител, обладающих высокой аффинностью к определенному антигену, — феномен, известный как созревание аффинности. В этих клетках также может происходить переключение изотипа. В-клетки, прошедшие этап селекции в зародышевом центре, покидают лимфоидный орган и продуцируют антитела того класса, который необходим.
В-клетки, активированные в зародышевом центре, в процессе дифференцировки также могут становиться В-клетками памяти (см. также рис. 7.1), которые покидают лимфоидный орган и перемещаются в ткани. Как именно В-клетки развиваются в зародышевом центре, в настоящее время не ясно, но считается, что плазматические клетки не становятся клетками памяти. В-клетки памяти являются непролиферирующими, обычно долгоживущими клетками, которые могут быть активированы в процессе последующего (повторного) более быстрого ответа на антиген. Эти клетки экспрессируют на своей поверхности изотипы, отличные от IgM и IgD, а именно IgG, IgA и IgE.
В-клетки памяти, похоже, не экспрессируют на своей поверхности особых молекул, отличающих их от наивных или активированных зрелых В-клеток, зато экспрессируют более высокие уровни CD44, чем другие В-клетки; CD44 участвует в адгезии лимфоцитов к клеткам вне лимфатического узла.
Общим результатом описанных этапов дифференцировки является то, что организм создает постоянно пополняемую библиотеку В-клеток разной специфичности (репертуар), направленных против огромного множества антигенов.
Таким образом, ответ на действие антигена зависит от взаимодействия антигена с существующим клоном В-клеток, содержащихся в данной библиотеке. Однако большинство В-клеток из этого огромного репертуара за время своего существования никогда не взаимодействуют с антигеном. Неактивированные зрелые IgM+IgD+-В-клетки находятся в течение примерно 4 — 5 мес в селезенке, где хранятся как покоящиеся лимфоциты.
Анатомическое распределение В-клеток
Как говорилось ранее, дифференцировка В-клеток на ранних этапах происходит в костном мозге. Зрелые В-клетки током крови перемещаются во вторичные лимфоидные органы, преимущественно лимфатические узлы, селезенку и пейеровы бляшки кишечника. Если В-клетка не взаимодействует с антигеном, она или покидает лимфоидный орган через лимфатические сосуды и продолжает циркулировать, или погибает в нем. Если В-клетка взаимодействует с антигеном и хелперными Т-клетками, формируется зародышевый центр, как указано ранее.
Те В-клетки, которые превратились в плазматические клетки, секретирующие IgG, через лимфатическую систему мигрируют в костный мозг и продолжают синтезировать Ig. Плазматические клетки, секретирующие IgA, находятся в ткани слизистой оболочки. Миграция наивных В-клеток во вторичные лимфоидные органы, а В-клеток, активированных антигеном, и В-клеток памяти в другие ткани управляется посредством разных типов хоминг-взаимодействия, посвященных Т-клеткам.
В-1-клетки
Описанные ранее этапы дифференцировки формируют популяцию В-клеток, доминирующую в крови, лимфе и вторичных лимфоидных органах. Эти В-клетки являются В-2-клетками. Вторая популяция В-клеток, называемая В-1-клетками, описана у людей, мышей и других животных. У взрослых особей в селезенке и лимфатических узлах В-1-клетки представляют минорную (меньшую в количественном отношении) популяцию, но преобладают в перитонеальной и плевральной полостях. Как в действительности взаимосвязаны В-1- и В-2-клетки, до конца не выяснено. Похоже, В-1-клетки используют ограниченный набор V-генных сегментов для формирования своего репертуара. Для большинства, но не всех В-1-клеток характерна поверхностная экспрессия молекул CD5, которые не экспрессируются на В-2-клетках. CD5+-B-1-клетки преобладают при хроническом лимфоцитарном лейкозе.
При попадании в организм разных типов бактерий на ранней стадии первичного ответа В-1-клетки синтезируют преимущественно низкоаффинные полиспецифичные (т.е. обладающие реактивностью относительно многих разных антигенов) антитела IgM. Они осуществляют так называемый тимуснезависимый ответ на бактериальные полисахариды, т.е. не нуждаются в Т-хелперах, чтобы синтезировать антитела.
В-1-клетки синтезируют IgM и малые количества (если вообще синтезируют) Ig других изотипов. По этим причинам считается, что В-1-клетки важны в качестве первой линии обороны против многих патогенов, особенно в иммунной системе слизистых оболочек. Кроме того, полагают, что В-1-клетки отвечают за синтез большинства «естественных» антител, которыми являются в основном антитела IgM, обнаруживаемые у индивидуума в отсутствие примирования антигеном.
Мембранные белки В-клеток
Главной особенностью В-клеток является способность синтезировать антитела после стимуляции антигеном. Продукция антител В-клетками, как будет более детально описано в следующих главах, является многоступенчатым процессом, требующим тесного взаимодействия В- и Т-клеток. На рис. 7.5 кратко описаны некоторые мембранные белки В-клеток, необходимые для синтеза антител, и другие белки, обладающие важными функциями.

Рис. 7.5. Важные молекулы, экспрессируемые на поверхностной мембране зрелой В-клетки
Антигенсвязывающие молекулы: мембранный иммуноглобулиновый рецептор
Передача сигналов молекулами, ассоциированными с мембранным иммуноглобулиновым рецептором
Тяжелые и легкие цепи Ig обладают очень короткими внутриклеточными доменами и непосредственно не передают сигнал в В-клетку после связывания с антигеном. Более вероятно, что ранее описанные молекулы Igα (CD79a) и Igβ (CD79b), нековалентно ассоциированные с Н- и L-цепями Ig на мембране В-клеток (см. рис. 7.2), передают сигнал активации внутрь В-клетки. Одним из самых первых событий, происходящих при активации В-клетки после связывания антигена с BCR, является фосфорилирование (добавление фосфатной группы) к остаткам тирозина в цитоплазматических участках Igα/Igβ ферментами протеинтирозинкиназами.
В Igα/Igβ тирозиновые остатки содержатся в аминокислотных последовательностях, относящихся к иммунорецепторной тирозинсодержащей активационной последовательности (мотиву) (immunoreceptor tyrosine-based activation motif — ITAM). Аминокислотная последовательность рассматривается как мотив, поскольку она обнаруживается в ряде других передающих сигнал молекул на клетках иммунной системы (например, связанных с Т-клеточными рецепторами).
Другие молекулы на мембране В-клетки влияют на сигнал, передаваемый через BCR, и таким образом играют важную роль в его передаче внутрь В-клетки. Гены CD19, CD81 (известный также как ТАРА-1) и CD21 ассоциированы в комплекс, называемый В-клеточным корецептором. Связывание антигена с корецептором усиливает активационный сигнал, передаваемый через BCR. Поэтому если антиген связывается к корецептором, требуется гораздо меньшее количество антигена, чем при активации В-клетки только через BCR. Корецептор со сходной функцией ассоциируется и с Т-клеточным рецептором.
В В-клеточном корецепторном комплексе CD21 является рецептором для компонента комплемента C3d, который связывается с микробными патогенами. Поэтому считается, что CD21 играет большую роль в усилении В-клеточных ответов на патогены, которые активируют каскад комплемента. Также CD21 действует как рецептор для вируса Эпштейна — Барр, что определяет возможность инфицирования В-клеток и их пролиферацию в ответ на действие вируса. Этот вирус является возбудителем мононуклеоза и лимфомы Беркитта в Африке (африканская лимфома).
Некоторые молекулы, экспрессированные на поверхности В-клеток, оказывают негативное действие при активации В-клетки. К ним относится рецептор CD22, который отрицательно регулирует корецепторы CD19, CD81 и CD21, а также CD32, являющийся низкоаффинным рецептором к Fc-фрагменту IgG (FcyRII) и экспрессирующийся практически на всех зрелых В-клетках. Рецептор CD32 связывает IgG, когда его агрегация происходит в отсутствие антигена и когда IgG находится в комплексе антиген—антитело. Рецептор CD32 играет важную роль в осуществлении антителами обратной связи — инактивации В-клетки путем подачи ей отрицательного сигнала.
Молекулы, участвующие во взаимодействиях Т- и В-клеток
Для активации Т-клеток антиген должны представлять антигенпрезентирующие клетки (АПК). В-клетки, особенно активированные, могут выступать в качестве АПК для Т-клеток. Они обладают важными чертами, присущими АПК.
Во-первых, В-клетки экспрессируют на своей поверхности белки, являющиеся молекулами главного комплекса гистосовместимости (МНС) II класса. Эти белки играют важнейшую роль в презентировании антигена большой субпопуляции Т-клеток, называемых СD4+-Т-клетками. В отличие от образцов экспрессии на многих других клетках экспрессия молекул МНС II класса на В-клетках является конститутивной, т. е. эти молекулы всегда экспрессируются. Экспрессия молекул МНС II класса на В-клетках может быть в дальнейшем увеличена при воздействии определенных цитокинов, таких как IL-4. Молекулы МНС II класса экспрессируются на всех клетках В-клеточной линии за исключением про-В-клеток.
Во-вторых, В-клетки экспрессируют высокие уровни семейства молекул, известных как В7 (CD80/CD86), которые относятся к костимулирующим молекулам, поскольку их присутствие, как и присутствие антигена, необходимо для активации наивных (непримированных) Т-клеток. Покоящиеся зрелые В-клетки экспрессируют низкие уровни В7 и являются слабыми АПК, тогда как активированные В-клетки — очень эффективными.
В-третьих, В-клетки экспрессируют CD40, который взаимодействует с CD154 (CD40-лиганд — CD40L), экспрессируемым на активированных Т-клетках. Это взаимодействие активирует В-клетки и играет основную роль в переключении изотопа, описанном ранее. Важность взаимодействия CD40 — CD154 подчеркивается таким состоянием, как Х-сцепленный гипер-IgM-синдром. У мальчиков с мутацией гена CD154, у которых Т-клетки либо вообще не экспрессируют, либо имеют нефункциональные гены CD154, вырабатываются только антитела IgM, а в их В-клетках не происходит переключения на другие изотипы.
Выводы
1. У млекопитающих на протяжении всей жизни ранние стадии дифференцировки В-клеток проходят в костном мозге. Самой первой из идентифицируемых клеток В-линии является про-В-клетка; на этой стадии происходит первая реаранжировка гена Н-цепи lg: Dн-генный сегмент реаранжируется к JH-генному сегменту.
2. Следующая стадия представлена пре-В-клеткой, у которой \/н-генный сегмент реаранжируется к объединенным DJ-сегментам, формируя VDJ-структуру, которая приближена Сμ-гену. В пре-В-клетке блок генов VDJСμ транскрибируется и транслируется, что ведет к синтезу μ-цепи. Эта цепь экспрессируется на поверхности пре-В-клетки в ассоциации с суррогатными легкими цепями.
3. На поверхности пре-В-клетки μ-цепь и суррогатные легкие цепи экспрессируются с двумя тесно связанными трансмембранными молекулами: Iga (CD79a) и lgβ (CD79b). Комплекс из μ- и суррогатных легких цепей в соединении с Iga и Igβ составляет пре-В-клеточный рецептор.
4. На следующей стадии дифференцировки начинают реаранжировать гены L-цепи; синтез суррогатных легких цепей прекращается; формируется к- или λ-цепь, которая ассоциируется с μ-цепью. Это приводит к формированию молекулы IgM, которая экспрессируется на поверхности клетки. Такая клетка относится к незрелым В-клеткам.
5. Если незрелая В-клетка встречается с антигеном, она обычно инактивируется. Взаимодействие незрелых клеток с собственными молекулами организма, приводящее к инактивации или устранению клеток с потенциальной аутореактивностью, — один из важнейших путей поддержания состояния аутотолерантности (негативная селекция).
6. На следующей стадии дифференцировки зрелые В-клетки экспрессируют IgM и IgD (с одинаковой антигенной специфичностью) на поверхности клетки.
7. Дальнейшее развитие зрелых В-клеток происходит преимущественно вне костного мозга и определяется контактом с антигеном. Активация В-клеток ведет к пролиферации и дифференцировке в плазматические клетки, которые синтезируют и секретируют антитела. Во время первичного ответа после контакта с антигеном синтезируются преимущественно IgM.
8. В-клетки, взаимодействующие с Т-клетками и их продуктами — цитокинами, осуществляют переключение изотипа (класса), т.е. продуцируют антитела различных изотипов: IgG, IgA, или IgE. Переключение изотипа включает механизм реаранжировки, характерный только для В-клеток: VDJ-структура тяжелой цепи, присоединенная к Сμ- и Сδ-генам, реаранжируется, чтобы присоединить другой ген С-области, такой как Cγ, Сα или Сε. В-клетка, которая синтезировала IgM и IgD, теперь может синтезировать антитела различных изотипов (IgG, IgA или IgE), но той же антигенной специфичности.
9. Соматический гипермутагенез генов, кодирующих V-области антител, происходит в зародышевых центрах вторичных лимфоидных органов. Это ведет к тому, что селектируются В-клетки с мутациями в области иммуноглобулиновых V-генов, кодирующие антитела с более высокой аффинностью к антигену, чем исходные В-клетки (созревание аффинности). Эти отобранные В-клетки могут развиваться в В-клетки памяти или плазматические клетки.
10. У отдельной В-клетки Н-цепь кодируется сегментами гена Н-цепи, находящимися либо на материнской, либо на отцовской хромосоме; L-цепь также кодируется сегментами гена L-цепи, находящимися на одной или другой хромосоме. Этот феномен использования генов только на одной хромосоме для синтеза Н-цепи lg называют аллельным исключением; он обеспечивает продукцию отдельной В-клеткой lg только одной антигенной специфичности.
11. Экспрессия мембранной формы lg присуща только В-клеткам. Молекулы Igα и Igβ, а также другие молекулы, ассоциированные с мембранным иммуноглобулиновым рецептором, после связывания антигена с lg передают сигнал в В-клетку. Та также экспрессирует на своей клеточной поверхности ряд молекул, играющих решающую роль во взаимодействии с другими клетками, особенно Т-клетками. Такими молекулами являются и молекулы МНС II класса, В7 и CD40.
источник