Путь кислорода в теле. Прием гемоглобином кислорода
В предыдущей статье мы рассмотрели, как кислород прошел альвеолярно-капиллярную мембрану и проник в кровеносный сосуд. Здесь он встречается с гемоглобином, который должен транспортировать его к клеткам. Читайте последовательно, или переходите по ссылкам.
И ВОТ О2 ПРОНИКАЕТ В КРОВЬ..
Часть II. Транспорт кислорода.
Гемоглобин
У крови много функций. Главная из них — перенос кислорода. Доставить весь кислород от легких к тканям в виде физически растворенного газа в крови невозможно — в плазме крови растворяется всего 3 %, так как кислород почти не растворяем в плазме и воде [ 1 ]. Поэтому для его транспортировки организм выделяет специфический белок крови — гемоглобин (Hb).
Гемоглобин находится в красных кровяных клетках, которые на греческом языке называются «эритроциты». Общая поверхность всех циркулирующих в крови эритроцитов 3800 м 2 .
Количество физически растворенного в крови кислорода мало и не играет значимой роли в его транспорте: при paO2 100 мм рт. ст. в литре крови O2 растворено всего 3,1 мл/л (СO2 – 45 мл/л). Если бы гемоглобина не существовало, адекватная доставка кислорода была бы возможной лишь при сердечном выбросе, превышающем 120 л/мин! [ 2 ] Однако эти 3 % важны, поскольку кислород из альвеол в кровь и эритроцит, и из капилляров к тканям проходит через физическое растворение.
Основное количество O2 переносится в связанном с гемоглобином виде.
Связывание кислорода гемоглобином (Нb + O2 = НbO2) происходит в капиллярах легких. В основном это получается за счет высокого парциального давления О2 в альвеолах (100 мм рт. ст.). Скорость прохождения крови в капиллярах легких, в среднем, составляет 0,5 с, но скорость оксигенации еще быстрей — всего 0,01 с.
Степень нормального насыщения кислородом артериальной крови 98 – 100 %. Но бывает и так, что кислородная емкость крови слишком мала. Тогда говорят о малокровии (анемии). Причина — нехватка эритроцитов в крови, или недостаток гемоглобина в эритроците. Это ситуация, когда желающих «сесть на поезд» много, а вагонов или мест в них мало.
Недостаток эритроцитов в крови
Причин недостаточного количества эритроцитов в крови может быть множество:
· Недостаточное образование эритроцитов — дефицит белка, железа, фолиевой кислоты, витамина B12 и др. Дефицит может быть при недостаточном поступлении с пищей или при нарушении их усвоением желудком и кишечником.
В каждой молекуле гемоглобина 4 атома железа, а всего его в организме около 4,5 г. За сутки мужчины теряют около 1 мг железа, а женщины — до 3 мг. В период менструаций потери возрастают до 14 мг. В период беременности потери составляют в сумме 700-800 мг, а за весь период лактации — 400 мг. Поэтому и мужчинам, и, особенно, женщинам, необходима постоянная компенсация железа.
· Дефицит железа в пище или низкая его усвояемость приводят к развитию железодефицитной анемии. Она часто встречается у женщин при беременности. При этом снижаются цветовой показатель ниже 0,8, уровень эритроцитов — ниже 3,6×1012/л, гемоглобин — ниже 110 г/л. [ 3 ];
· Разрушение эритроцитов раньше срока. В норме срок жизни эритроцита 120 дней. Инфекции, вирусы и грибки сокращают срок его службы (см. ниже);
· Беременность. Эстрогены тормозят эритропоэз, поэтому в период беременности уровень эритроцитов часто снижен (присутствует анемия) [ 4 ];
· Наследственное генетическое заболевание крови;
· Кровопотеря. Количество эритроцитов в крови сокращается в результате острой или хронической кровопотери – ранения, кровоточащая язва желудка, геморроидальные узлы и др.;
· Прием некоторых препаратов. Например, фенобарбитал является частью популярных сердечных и успокоительных средств (корвалол и др.). При частом использовании может привести к эритропении. Неблагоприятное воздействие на эритроциты оказывает химиотерапия.
Недостаток гемоглобина в эритроцитах
Теперь рассмотрим ситуацию, когда в крови достаточно эритроцитов, но концентрация общего гемоглобина ниже нормы.
В одном эритроците 270 миллионов молекул гемоглобина. Если микроскоп показывает мембраны эритроцитов однородной окраски — в них 100 % содержание гемоглобина. Но очень часто можно встретить внутри эритроцита белое кольцо, которое лишь снаружи окрашено в розовый цвет — в нем гемоглобина всего 50-60 %, то есть меньше чем у здорового эритроцита. Если таких эритроцитов будет более 30 %, показатель общего гемоглобина снижается, и врачи ставят диагноз анемия.
Люди, страдающие анемией бледны, словно им и в самом деле не хватает крови. При недостатке гемоглобина кровь несет тканям недостаточное количество кислорода и в них возникает гипоксия. В результате производится меньше энергии, и люди быстрее устают.
Почему не хватает гемоглобина в эритроцитах?
· Гемоглобин это белок. Дефицит белка означает, что у этого человека в рационе питания мало качественного белка.
· Агрессия вирусами, грибками, паразитами и прочими простейшими. При осмотре через микроскоп, на это указывают неровные края мембраны эритроцита, что указывает на его повреждение. Еще можно увидеть, как к мембране эритроцита прикрепляются нитиевидные образования, которые используют его как сырьевую базу. Гемоглобин едят грибки, вирусы и паразиты, они любят его, он для них он важен. [ 5 ]
· Молекула гемоглобина состоит из 514 аминокислот, из которых 7 в организме не синтезируются. Они должны поступить в наше тело только с едой. Обзор необходимых аминокислот для высокого гемоглобина см. здесь.
· Некоторые люди по наследству через гены получают заболевание крови — гемоглобиноз, при котором гемоглобин имеет низкую способность транспортировать кислород.
Бывает и обратная ситуация, при которой в крови образуется слишком большое количество эритроцитов. Это состояние называется полицитемией (от греч. «много клеток в крови»). Слишком много эритроцитов сгущает кровь, делает ее более вязкой. Это препятствует нормальной циркуляции крови и насыщению кислородом тканей.
Когда человек живет высоко в горах, полицитемия только желательна, но на уровне моря она может стать опасной. Поэтому спускающиеся с гор люди проходят акклиматизацию, как и равнинный житель в горах, только здесь наоборот.
Дисгемоглобин
Осталось рассмотреть еще одну ситуацию, которая может помешать кислороду зайти в эритроцит. Это тот случай, когда поезда в расписании есть, билет куплен, но увы, место занято другим пассажиром.
Гемоглобин собирает исключительно молекулы кислорода («на этом поезде места для тех кто купил билеты»). Однако некоторые газы могут этому помешать — это дисгемоглобины («хулиганы без билетов»). Слишком высокая концентрация дисгемоглобинов (COHb и MetHb) приводит к падению активной и эффективной концентрации гемоглобина и, соответственно, к гипоксии.
При отравлении угарным газом образуется карбоксигемоглобин (COHb), а при отравлении гипербарическим кислородом — метгемоглобин (MetHb). Карбоксигемоглобин и метгемоглобин не способны присоединять и транспортировать кислород.
· Отравление угарным газом (СО, окись углерода). Если при недостатке кислорода сжечь углеродсодержащее вещество, например, уголь или бензин, образуется угарный газ. Попадая в кровь с дыханием, молекула гемоглобина присоединяет к себе угарный газ вместо кислорода, и становится бесполезной для дыхания клеток. Способность присоединяться к гемоглобину у угарного газа в 300 раз выше, чем у кислорода, а его отделение от гемоглобина происходит в 10 000 раз медленнее, чем у кислорода [ 6 ].
Если угарный газ вывел из строя небольшое количество гемоглобина, последствия не будут серьезными. Но угарный газ имеет отвратительное свойство, которое делает его особенно опасным — цепляясь к атому железа, СО создает трудноразъединимое соединение — карбоксигемоглобин (Нb + СO = НbСO). В отличие от молекулы кислорода, он не может легко освободиться от гемоглобина, когда кровь завершает свой круг в организме и возвращается в легкие. Происходит процесс накопления.
И хотя содержание угарного газа в воздухе мало, со временем большая часть гемоглобина в крови начинает циркулировать впустую. Если в воздухе содержится 0,1 % CO, то около 80 % Hb крови превращается в НbСO. Карбоксигемоглобин не может связывать кислород, и в итоге постепенно развивается удушье.
Угарный газ попадает к нам в организм с выхлопным дымом автомобилей, выбросом промышленных предприятий, с сигаретным дымом и др.
В норме содержание НbСO в крови составляет 1 %. У курильщиков НbСO значительно выше — после выкуренной сигареты его содержание может возрасти до 5 % и более, а к вечеру доля НbСO может возрасти до 20 % общего гемоглобина в крови. [ 7 ] При содержании в крови 20 – 25 % НbСO человеку требуется специфическая врачебная помощь: дать чистый кислород, желательно под повышенным давлением.
· Сильные окислители. При действии сильных окислителей О2 может образовывать прочную химическую связь с железом гема, при которой атом железа становится трехвалентным. Такое соединение гемоглобина с кислородом называют метгемоглобином. Метгемоглобин не высвобождает кислород в тканевых капиллярах.
Метгемоглобинемия может быть врожденной, или развиться в результате некоторых видов острых химических отравлений (анилиновые красители, парацетамол, перманганат калия и пр.). Даже в обычных условиях у здоровых людей до 3 % гемоглобина крови может быть в виде метгемоглобина из-за постоянного поступления в кровь окислителей — перекиси, нитропроизводных органических веществ и др.
· Другие вещества. Гемоглобин легко взаимодействует и со многими другими растворенными в крови веществами. В частности, при взаимодействии с лекарственными препаратами, содержащими серу (например, принятие серных ванн), может образовываться сульфгемоглобин, сдвигающий кривую диссоциации НbO2 вправо.
Сатурация
Когда кислород (O2) соединяется с гемоглобином (Hb), он становится оксигемоглобином (HbO2). Кровь при этом приобретает ярко-алый цвет, что типично для артериальной крови. Венозная кровь содержит меньше кислорода, поэтому её цвет более темный.
У гемоглобина, как у транспортного белка, две задачи: присоединять кислород в легких и отдавать его тканям. Эти задачи противоположны по своей сути, но выполняются одним и тем же веществом. Поэтому стремление гемоглобина связываться с кислородом должно быть достаточным, чтобы обеспечить кровь кислородом, но не избыточным, чтобы не нарушить процесс отдачи кислорода клеткам.
Для обозначения меры насыщения кислорода гемоглобином, был придуман термин — сатурация (SO2). Динамическая взаимосвязь SO2, и давления кислорода в крови (pO2), дает кривую диссоциации HbO2 (рис. 1).
Середину этой кривой отметили точкой, при которой 50 % молекул гемоглобина связаны кислородом — это называют парциальным напряжением полунасыщения и обозначают как P50 (рН 7,4 температура 37 °С).
Увеличение P50 говорит о снижении сродства гемоглобина к кислороду, а его снижение — о возрастании.
Рис. 1-1; 1-2. Кривая диссоциации оксигемоглобина и ее характеристики:
А — кривая диссоциации оксигемоглобина и содержание кислорода в крови;
Б — смещение кривой диссоциации оксигемоглобина (сдвиг P50) облегчает захват O2 в легких и способствует диссоциации Hb – O2 на уровне тканей.
На «артериальной» части кривой существенное изменение PaO2 сопровождается незначительным сдвигом SO2. На «венозном» сегменте, напротив, небольшие изменения PO2 сопряжены с выраженным отклонением SO2
Напряжение кислорода (рО2)
Парциальное давление, или напряжение — выступает в качестве движущей силы перемещающей оксигемоглобин (HbO2) в организме. На протяжении всего пути кислорода, он будет перемещаться из зоны более высокого давления, в более низкую.
В атмосфере парциальное давление кислорода 150 – 160 мм рт. ст., а в конечной точке его путешествия — контуре респиратора митохондрии — pО2 всего 1 – 3 мм рт. ст. Таким образом, при прохождении кислорода к клеткам напряжение кислорода последовательно снижается, поскольку каждый этап транспорта связан с существенными издержками. Это явление получило название «кислородного каскада» (рис. 2).
Рис. 2. «Кислородный каскад». Описывает падение парциального давления кислорода, начиная от атмосферного воздуха и заканчивая мембраной митохондрий, конечного получателя кислорода.
Давайте посмотрим как это работает. Вдохнув воздух, парциальное давление кислорода в котором составляет 158 мм рт. ст., он попадает в верхние дыхательные пути, где нагревается и увлажняется. При прохождении области водяных паров (до 100 % относительной влажности), давление падает до 148 мм рт. ст. [ 8 ]
В альвеолах кислород смешивается с покидающим организм углекислым газом, что в обычных условиях уменьшает давление PO2 в альвеолярном воздухе до 103 – 107 мм рт. ст. Его могут уменьшить загрязнения вдыхаемого воздуха различными газами или нарушения легочной вентиляции [ 9 ], мы об этом говорили выше.
Потеря давления кислорода на альвеолярно-капиллярной мембране невелика — всего 1 мм рт. ст. Внутрилегочное шунтирование в артериальную кровь снижают PO2 до 90 – 100 мм рт. ст. В капиллярах тканей напряжение О2 падает до 40 мм рт. ст. Здесь кислород поступает в клетки органов и тканей — на поверхностях клеток парциальное давление составляет около 20 мм рт. ст., а в клеточных митохондриях — около 1 %. Когда PO2 в клетке становится равным 0,1 мм рт. ст. клетка погибает. [ 10 ]
Как мы видим, потеря кислорода может происходить на каждой из ступеней каскада.
Кроме парциального давления кислорода, на связывание гемоглобином кислорода влияют ряд вспомогательных факторов: напряжение углекислого газа (раCО2); температура легких (t °C); увеличение рН крови (эффект Вериго-Бора); и содержание в эритроците 2,3-ДФГ. Рассмотрим их.
Напряжение углекислого газа (раCО2)
Кроме транспорта кислорода к тканям, гемоглобин осуществляет обратный транспорт из клеток их конечного газового метаболита — углекислого газа (СО2). Содержание СО2 в венозной крови составляет 15 – 20 % [ 11 ].
Венозная кровь отдает альвеолам СО2, в результате чего в крови легочных капилляров снижается парциальное давление углекислого газа (рСО2). Это повышает сродство гемоглобина к кислороду, что приводит к насыщению артериальной крови кислородом.
В нормальных условиях у человека, при t 37 °С, рН 7,40 и pСO2 = 40 мм рт.ст. – p50 = 27 мм рт.ст.
Температура в лёгких
Реакция насыщения кислородом (оксигенации) гемоглобина, как и большинства химических реакций в организме, зависит от температуры. Мы это видели на примере работы ферментов. Оптимальная температура тела, является ключевым условием для поддержания Здоровья.
При понижении температуры легких присоединение О2 к гемоглобину ускоряется. Мы видим что с падением температуры кривая диссоциации НbО2 сдвигается влево (см. рис. 3). В этом случае гемоглобин активнее захватывает кислород, но в меньшей мере отдает его тканям.
Рис. 3. Кривые диссоциации оксигемоглобина:
а) — при одинаковой температуре (Т = 37 °С) и различном парциальном давлении углекислого газа (pCO2);
б) — при одинаковом pCO2 (40 мм рт. ст.) и различной температуре.
По вертикали отмечен процент молекул гемоглобина связанных с кислородом (НbO2), а по горизонтали — уровень напряжения кислорода (рO2).
Содержание в эритроците 2,3-ДФГ
2,3 Дифосфоглицерат (ДФГ) является промежуточным продуктом бескислородного производства АТФ (см. гликолиз). 2,3-ДФГ служит некоторой защитой от гипоксии в случае снижения поступления кислорода при ситуациях подъема в горы на высоту свыше 3-х км над уровнем моря, при хронических заболеваниях легких, сердечной недостаточности с цианозом, недостатка гемоглобина и других патологических причин, которые снижают поступление кислорода клеткам.
Например, при дыхательной недостаточности наблюдается резкий подъем уровня 2,3-ДФГ, который сохраняется на протяжении всего срока заболевания. Есть взаимосвязь между степенью тяжести дыхательной недостаточности, выраженностью дыхательной гипоксемии и уровнем 2,3-ДФГ.
В случаях нехватки кислорода в тканях, синтез 2,3-ДФГ в эритроцитах увеличивается, и отделение О2 от НbO2 ускоряется, что частично компенсирует кислородный голод тканей. У пожилых людей содержание 2,3-ДФГ в эритроцитах повышено, что указывает на отчаянную попытку организма препятствовать развитию гипоксии тканей.
Процесс старения сопровождается появлением новых качеств, направленных на сохранение компенсаторных механизмов, однако они лишь в неполной мере поддерживают процессы адаптации [ 12 ].
У тренирующих выносливость спортсменов, концентрация 2,3-ДФГ в эритроцитах на 15 – 20 % выше, чем не у спортсменов [ 13 ]. В норме содержание 2,3-ДФГ в сыворотке крови составляет 1,6 – 2,6 ммоль/л.
В крови мужчин уровень эритроцитов в норме 4 – 5,1 х1012/л, в крови женщин — 3,7 – 4,7х1012/л.
В норме уровень гемоглобина у мужчин 130 – 160 г/л, у женщин — 115 – 145 г/л. Обычно его определяют с помощью гемометра Сали, но этот метод дает до 30 % ошибку, поэтому лучше использовать гемоглобинцианидный или другие методы. [ 14 ]
Содержание оксигенированного гемоглобина (НbО2) в артериальной крови выше 94 % считается нормой. При содержании 90 % ткани испытывают кислородное голодание и необходимо принимать срочные меры, улучшающие доставку в них кислорода.
Если мы не живем высоко в горах, у нас нет хронических болезней легких, и наши альвеолы не забиты пылью и табачной смолой, при этом у нас сбалансировано питание, хороший гемоглобин, мы не работаем в холоде и дышим воздухом без превышения ПДК — нам не стоит особенно волноваться о проблеме насыщения гемоглобина кислорода пришедшего из лёгких.
Большинство людей всегда имеет высокое насыщение крови кислородом — содержание НbО2 в возвращающейся из капиллярной сети в легкие венозной крови составляет 67 – 75 % [ 15 ]. Как увеличить отдачу тканям уже имеющегося кислорода в крови — вот задача достойная самого пристального нашего внимания. Как это делают термальные бикарбонатные ванны, мы узнаем чуть дальше.
Сейчас мы остановились на том, что НbО2 должен «доехать» до места назначения — например, к мизинцу левой ноги. Успех его доставки будет зависеть от состояния кровеносных сосудов и густоты крови. Давайте это рассмотрим прямо сейчас.
источник
Сколько молекул кислорода присоединяет одна молекула гемоглобина
14.13.1. Транспорт кислорода
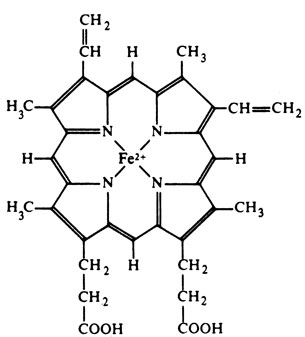
Кислород переносят молекулы гемоглобина, содержащиеся в эритроцитах. Гемоглобин представляет собой тетрамерный белок с мол. массой 68000. В его состав в качестве простетических групп входят четыре молекулы гема, которые присоединены к четырем полипептидным цепям глобина и придают крови характерный красный цвет. Каждый гем содержит один атом двухвалентного железа, непрочно связывающего одну молекулу кислорода (рис. 14.62):
Рис. 14.62. Строение молекулы гема
Присоединение кислорода к гемоглобину с образованием оксигемоглобина происходит при высоком парциальном давлении кислорода-таком, как в капиллярах легочных альвеол. При низком парциальном давлении кислорода (как в капиллярах метаболически активных тканей) связь между кислородом и гемоглобином становится непрочной, кислород освобождается и диффундирует в окружающие клетки.
Количество кислорода, которое может связаться с гемоглобином, зависит от напряжения кислорода в среде. Последнее выражают как парциальное давление кислорода в атмосфере, находящейся в равновесии с данной средой. Парциальное давление до сих пор выражают в миллиметрах ртутного столба. Например, атмосферное давление на уровне моря составляет 760 мм рт. ст. Кислород составляет около 1/5 атмосферного воздуха; следовательно, его парциальное давление на уровне моря равно примерно 1/5⋅760 = 152 мм рт. ст.
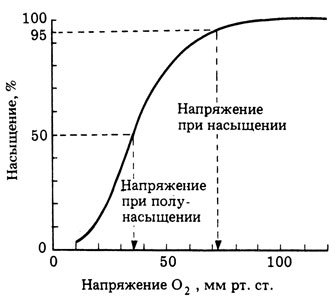
Определяя процент насыщения крови кислородом при различном парциальном давлении O2, получают S-образную кривую, называемую кривой диссоциации оксигемоглобина (рис. 14.63).
Рис. 14.63. Этот график поясняет термины, принятые для описания кривых диссоциации пигментов, переносящих кислород. Напряжение насыщения — это то напряжение кислорода, при котором насыщено кислородом 95% пигмента, а напряжение полунасыщения — то, при котором насыщено кислородом 50% пигмента. (Из Florey, An introduction to general and comparative physiology, 1966, W. B. Saunders and Co.)
Анализ этой кривой показывает, что в физиологическом плане гемоглобин можно считать полностью насыщенным кислородом при таком напряжении О2, при котором фактически насыщается 95% гемоглобина. В примере, приведенном на рис. 14.63, такое напряжение составляет около 73 мм рт. ст. При более высоком парциальном давлении О2 может происходить дальнейшее его поглощение, но 100%-ное насыщение гемоглобина достигается редко. При парциальном давлении кислорода около 30 мм рт. ст. только 50% гемоглобина находится в форме оксигемоглобина, а при нулевом парциальном давлении О2 молекулы гемоглобина вообще не связывают кислород. В области крутого наклона кривой уже при небольшом снижении парциального давления О2 процент насыщения гемоглобина значительно уменьшается. Кислород, освобождаемый пигментом, становится доступным для тканей.
Почему же кривая насыщения имеет S-образную форму? Такая форма кривой объясняется аллостерическим характером взаимодействия гемоглобина с кислородом (разд. 6.6). Когда молекула О2 связывается с атомом двухвалентного железа одного из гемов, конфигурация этого гема слегка изменяется. Это изменение отражается на конфигурации всей молекулы гемоглобина, которая определенным образом меняется. По мере присоединения кислорода к второй и третьей группам гема происходит дальнейшее изменение конфигурации гемоглобина, и в результате каждая последующая молекула О2 присоединяется легче, чем предыдущая (явление кооперативности), так что последний гем связывает кислород в несколько сотен раз легче, чем первый.
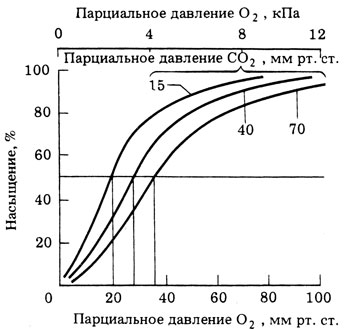
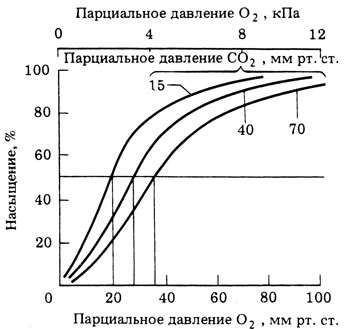
Обратный процесс происходит тогда, когда оксигемоглобин оказывается в области низкого парциального давления О2, как это бывает в активно дышащих тканях. Первую молекулу кислорода оксигемоглобин отдает тканям очень легко, но вторая, третья и четвертая молекулы отделяются значительно труднее и только при очень сильном снижении парциального давления O2. При повышении парциального давления СО2 кривая диссоциации оксигемоглобина сдвигается вправо, и это явление называют эффектом Бора (рис. 14.64).
Рис. 14.64. Кривые диссоциации оксигемоглобина при различном парциальном давлении СО2, иллюстрирующие эффект Бора. (Из Garth Chapman, The body fluids and their function, Studies in Biology, № 8, 1967, Arnold.)
14.37. Каково физиологическое значение эффекта Бора?
14.38. Рассмотрите рис. 14.65. Кривая диссоциации оксигемоглобина у плода сдвинута влево по сравнению с кривой для матери. Чем объясняется такое смещение?
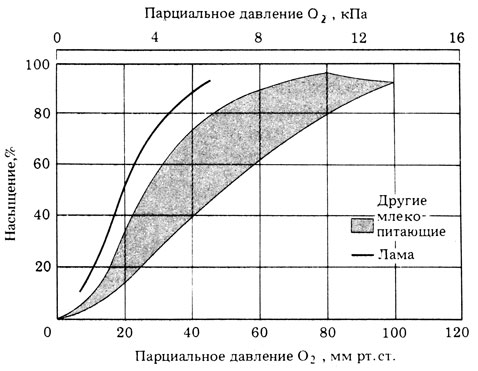
14.39. Кривая диссоциации оксигемоглобина у южноамериканских лам, живущих в Андах на высоте около 5000 м над уровнем моря, расположена левее, чем у большинства других млекопитающих (рис. 14.66). Чем это можно объяснить?
Рис. 14.65. Кривые диссоциации оксигемоглобина в крови плода и матери у овцы
Рис. 14.66. Сравнение кривых диссоциации оксигемоглобина у ламы и других млекопитающих
Собираетесь получить наибольшее многообразие в сексе? Всегда очаровательные проститутки имеют очень большой спектр услуг интимного характера, которыми вы при влечении можете попользоваться в абсолютно любое время дня и ночи.
источник