Фракции гемоглобина
Около 7% мирового населения являются носителями гемоглобинопатий. 300 –500 тыс. детей ежегодно рождаются с тяжелыми гемоглобинопатиями. До недавнего времени считалось, что Российская популяция не относится к группе риска по наследственным гемоглобинопатиям ввиду низкой распространенности данного вида нарушений у славянских народов. Однако растущая глобальная миграция привела к проникновению расстройств гемоглобинной системы во многие зоны, где первоначально они не были эндемичными.
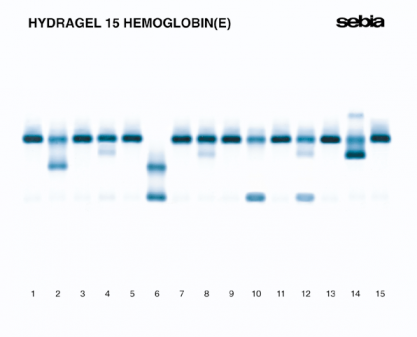
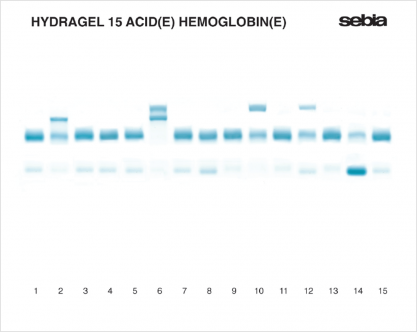
Электрофорез фракций гемоглобина применяется для диагностики наследственной патологии гемоглобинов – гемоглобинопатий, включая наследственно обусловленные анемии и талассемии. Для оценки всех вариантных форм гемоглобина электрофоретическое разделение в геле агарозы проводят в двух условиях: в щелочном и в кислом буфере. Это позволяет выявлять все описанные физиологические и патологические (свыше 1400) варианты гемоглобина и точную количественную оценку гемоглобина А2, направленную на диагностику β-талассемий. Методика позволяет провести четкое разделение гемоглобина F от гемоглобинов А и S; гемоглобинов С и Е от гемоглобина А2. Использование функции наложения контрольного профиля на профиль пациента позволяет провести идентификацию мигрирующих близко друг к другу гемоглобинов S и D.
Результаты. Разделение фракций гемоглобина в щелочных условиях позволяет выделить и количественно измерить фракции: Hb(А0+A1), HbF, Hb(S+D), Hb(A2+C+E). Разделение фракций гемоглобина в кислых условиях позволяет выделить и количественно измерить фракции: HbC, HbS, Hb(A0+A2+D+E), Hb(A1+F).
Материал для исследования: цельная кровь с антикоагулянтом K2ЭДТА или K3ЭДТА.
Пробоподготовка: ручная подготовка гемолизата.
Совместимость с прибором
№ по каталогу
Наименование набора
Кол-во тестов на набор
Белковые фракции гемоглобина в щелочных условиях
Белковые фракции гемоглобина ГИДРАГЕЛЬ (HYDRAGEL 7 HEMOGLOBIN(E))
Белковые фракции гемоглобина ГИДРАГЕЛЬ (HYDRAGEL 15 HEMOGLOBIN(E))
Белковые фракции гемоглобина в кислых условиях
Белковые фракции гемоглобина ГИДРАГЕЛЬ (HYDRAGEL 7 ACID(E) HEMOGLOBIN(E))
Белковые фракции гемоглобина ГИДРАГЕЛЬ (HYDRAGEL 15 ACID(E) HEMOGLOBIN(Е))
Контрольная сыворотка для электрофореза Hb A2 НОРМА (Hb A2 NORMAL CONTROL)
Контрольная сыворотка для электрофореза Hb A2 ПАТОЛОГИЯ (Hb A2 PATHOLOGICAL CONTROL)
Контрольная сыворотка для электрофореза Hb AF (Hb AF CONTROL)
Контрольная сыворотка для электрофореза Hb AFSC (Hb AFSC CONTROL)
Дополнительные реагенты и расходные материалы (по потребности)
Промывающий раствор для электрофореза ГИДРАЗИС (HYDRASYS WASH SOLUTION)
Обесцвечивающий раствор для электрофореза (DESTAINING SOLUTION)
источник
Причины снижения фракции гемоглобина а: методы лечения
Снижение фракции гемоглобина (Нb) может сопровождать многие заболевания крови, чаще всего это связано с наследственным заболеванием – талассемией. Фракции гемоглобина, которые различаются по аминокислотному составу, сродству к кислороду, углекислому газу, имеют 3 вида: А (Нb взрослых),Р (Нb плода), F (Нb новорожденного). На молекулярном уровне структура Нb состоит из цепей глобина, строение и количество которых нарушается при талассемии.
Что такое талассемия
Талассемия – наследственная гемоглобинопатия с изменением количественного состава альфа и бета глобиновых цепей, которые входят в структуру гемоглобина А. При генетическом заболевании из-за нарушения строения гемоглобина разрушается внешняя оболочка эритроцита, что приводит к гибели клеток, выходу ее содержимого в кровь, гемолитической анемии.
Патология альфа чаще встречается в странах Западной Африки, Южной Азии, бета в Средиземноморье, Индонезии, Северной Африке, где часто встречается малярия. Согласно статистике, в мире каждый год рождается около 300 тыс. детей с разными видами талассемии. Признаки патологии могут отсутствовать в одном поколении, в другом привести к летальному исходу.
Особенность талассемии в том, что она может выступать в виде защитного механизма против малярийного плазмодия.
Причины
Аномалия строения гемоглобина относится к наследственным аутосомно-рецессивным заболеваниям. В гене происходят мутации с изменением количества его цепей или их последовательности, которые влияют на синтез цепочек гемоглобина. На молекулярном уровне причиной является появление дефектной матричной рибонуклеиновой кислоты (РНК), нарушение транскрипции.
За счет этих нарушений синтез глобиновых цепей нарушается или полностью останавливается, формируется дефектный гемоглобин. Возможные причины молекулярных мутаций:
- вирусные болезни;
- влияние на организм химических мутагенов;
- наркотики;
- алкоголизм;
- противоопухолевые препараты;
- ионизирующая радиация.
Патология наследуется от родителей гомозиготно (получение мутированного гена от обоих родителей), гетерозиготно (дефектный ген достается ребенку от одного родителя).
Симптомы
Если мутированный ген унаследовался от одного родителя (гетерозиготно), симптоматика отсутствует либо болезнь проявляется слабо выраженными признаками в виде легкой анемии. Ее основные проявления – усталость, бледные кожные покровы. При диагностике выявляют незначительное увеличение селезенки, гипохромную анемию. Выраженные признаки заболевания наблюдаются, если дефектный ген передался от двух родителей (гомозиготно).
Чаще встречается бета-форма талассемии. Ее признаки проявляются в первый год жизни ребенка:
- изменение прикуса;
- переносица в виде седла;
- монголоидное лицо;
- изменение формы черепа (башенный, четырехугольный);
- увеличение печени, селезенки;
- землянисто-желтушный цвет кожи;
- патологические переломы костей при отсутствии травм;
- отставание в физическом развитии.
Возможно появление камней в желчном пузыре, воспаление суставов, язвенное поражение кожи ног. При талассемии разрушаются эритроциты, в крови повышается уровень железа, который может скапливаться в органах, вызывая цирроз печени, фиброзные изменения в поджелудочной железе, кардиосклероз, сахарный диабет.
Альфа-талассемия, связанная с получением 2 дефектных генов от обоих родителей не совместима с жизнью, плод погибает внутриутробно.
Классификация
В зависимости от вида поврежденной цепи выделяют альфа-, бета, дельта — , гамма-талассемию. Последние 2 вида встречаются редко. Каждый вид включает в себя несколько подвидов.
Альфа-талассемия
Возникает из-за нарушения количества, структуры цепей альфа-глобина. Чем больше поврежденных генов, тем меньше синтезируется альфа-глобинов.
Альфа-талассемия с одним поврежденным геном
У человека с одним мутированным геном уровень эритроцитов, гемоглобина, как правило, в пределах нормы, возможна гипохромная анемия. Признаки заболевания отсутствуют, но человек носитель мутированного гена, который он может передать своим детям. Если ребенок унаследует только 1 поврежденный ген, он также станет носителем. Если он получит по одной поврежденной глобиновой цепи от каждого родителя, то проявятся характерные признаки талассемии.
Альфа-талассемия с двумя поврежденными генами
Симптоматика маловыражена или отсутствует. В крови определяют микроцитарные эритроциты, снижение количества здоровых эритроцитов. Проявляются признаки хронической анемии, выраженность которой не уменьшается на фоне лечения железосодержащими препаратами. Подтверждают генетическую микроцитарную анемию путем исключения других причин анемического состояния, ДНК-исследованиями с выявлением 2-х поврежденных цепей, которые могут быть повреждены в одном или двух генах.
Повреждение 3 генов – болезнь гемоглобина Н
Из-за повреждения трех альфа-цепей увеличивается количество бета-цепочек, которые замещают альфа. Заболевание вызывает анемию средней, тяжелой степени с увеличением размеров селезенки. Клиническая картина разнообразна, несмотря на серьезные нарушения в строении гемоглобина возможно бессимптомное носительство, но при передачи гена потомству возникают тяжелые нарушения в организме.
Повреждение 4 генов – большая альфа-талассемия
Самая тяжелая форма нарушения альфа-глобина. При таком повреждении цепи не синтезируются, соответственно нарушено синтезирование нормального, фетального гемоглобина. В 80% случаев плод погибает внутриутробно. Рожденные с большой талассемией дети имеют аномалии развития органов, как правило, умирают в течение 2-3 лет.
Вета-талассемия
Связана с мутацией одного или нескольких генов, кодирующих бета-глобиновые цепи. Известно до 200 мутаций. Виды:
- Бета-талассемия с одним поврежденным геном – не проявляется характерными для патологии симптомами, возможно уменьшение размеров эритроцитов, анемия легкой степени.
- Промежуточная форма с двумя поврежденными генами – глобиновые цепи синтезируются, но их количество снижено. Проявляется анемией средней степени.
- Тяжелая форма, связанная с угнетением синтеза бета-цепей. Начинает проявляется с 3-х месяцев жизни. Вызывает анемию тяжелой степени.
Другие виды возникают, если мутированный ген бета-цепи сочетается с патологической формой гемоглобина. Наиболее значимыми являются 2 формы: НbЕ, НbS (серповидно-клеточная бета-талассемия).
Тяжелая форма бета-талассемии требует регулярных гемотрансфузий, медикаментозного лечения на протяжении всей жизни.
Диагностика
В постановке диагноза важен семейный анамнез, из которого можно узнать о случаях талассемии в роду. При физикальном исследовании обращают внимание на изменение строения черепа, костей носа, нижней челюсти, цвет кожи. При лабораторной диагностике при расшифровке общего, биохимического анализа крови для талассемии характерно:
- снижение уровня гемоглобина;
- изменение цветового показателя;
- высокий уровень непрямого билирубина;
- гипохромная анемия;
- эритроциты в форме мишени.
Чтобы определить фракции гемоглобина, содержание в крови его дефектных форм проводят электрофорез. При рентгенологическом исследовании черепа, трубчатых костей выявляют нарушения строения, формы костной ткани. При УЗИ возможно обнаружение камней в желчном пузыре, увеличение размеров печени, селезенки. Чтобы выявить мутированные гены проводят молекулярно-генетические исследования.
Лечение
Если клинические признаки талассемии не проявляются, лечение не требуется, чаще это касается бета-форм с наследованием гена от одного родителя. При рождении больного ребенка с двумя дефектными генами (по одному от каждого родителя) лечение требуется с первого месяца. Консервативная терапия включает в себя регулярные гемотрансфузии. Частоту процедур определяют по лабораторных показателям, выраженности симптомов, возрастным особенностям.
Для купирования периодов обострений талассемии назначают глюкокортикостероиды. Чтобы снизить уровень железа в крови показаны хелатирующие препараты. При талассемии снижается иммунитет, дети часто болеют инфекционными болезнями с осложнениями, поэтому назначают иммуномодуляторы, витаминные комплексы, вакцины против пневмококка.
Оперативное вмешательство показано при камнях в желчном пузыре, увеличение объема селезенки, которая сдавливает соседние органы. К хирургическому лечению относят пересадку костного мозга, если нарушается выработка форменных элементов. Для пересадки костного мозга подбирают только гистосовместимого донора.
Если верить статистике, примерно 1,5% мирового населения являются носителями β-талассемии без клинических симптомов. Профилактические мероприятия включают предупреждение браков между двумя носителями мутированных генов, проведение медико-генетических исследований при планировании ребенка, в период беременности. Для выявления нарушений строения гемоглобина необходимо дородовое инвазивное исследование (биопсия, забор амниотической жидкости).
источник
Причины и симптомы снижения фракции гемоглобина а: как лечить
Фракции гемоглобина (Нb) включают в себя 3 главных вида: Нb А ,Р,F. Они различны по составу аминокислот, свойствам, процентному содержанию в крови. Нb А – это основная фракция гемоглобина в крови взрослого человека (95%), Нb Р содержится в крови у плода до 5 месяца внутриутробной жизни, после образуется Нb F. На молекулярном уровне гемоглобин состоит из глобиновых цепей. Угнетение их синтеза приводит к тяжелым генетическим заболеваниям.
Что такое талассемия
Это наследственная, количественная гемоглобинопатия, которая связана с угнетением синтезирования белковых цепей альфа и бета, составляющих структуру гемоглобина А. Патология приводит к разрушению целостности оболочки эритроцита и его уничтожению. В гематологии заболевание относят к генетическим гемолитическим анемиям.
Заболевание распространено в странах Африки, Индии, Средней Азии, Индонезии, Закавказья и Ближнего Востока. С талассемией каждый год рождается примерно 300 000 детей. Патология может протекать в нескольких формах: бессимптомной, тяжелой, смертельной. Особенность талассемии в том, что она может развиваться как защитный фактор против малярии.
Талассемия переводится как «анемия морского побережья», поэтому она и распространена среди жителей Черноморского и Средиземноморского регионов.
Классификация
Виды патологии в зависимости от нарушения цепи гемоглобина:
- Альфа-талассемия, которая связана с подавлением синтезирования альфа-цепочек Нb. Патология включает: гемоглобинопатию Н, гетерозиготное носительство (при получении мутированного гена от одного родителя) и гомозиготную талассемию (при наследовании гена от двух родителей) в виде водянки плода с Нb Бартса.
- Бета-талассемия, связанная с угнетением синтезирования бета-цепей гемоглобина А. Форма включает гомо- и гетерозиготную талассемию бета и дельта.
- Гамма-талассемия, которая связана с подавлением образования гамма-цепей Нb.
- Дельта-талассемия – угнетение цепей-дельта.
Также наследственная патология включает в себя талассемию, развитие которой связано со структурными изменениями в строении Нb. Согласно классификации выделяют малую и большую талассемию, разница между ними в выраженности симптомов.
Причины
Патология относится к наследственным аутосомно-рецессивным заболеваниям. Главная причина – мутационные процессы в гене, который отвечает за синтезирование цепей Нb. В основе молекулярного дефекта лежит появление аномальной матричной РНК (рибонуклеиновой кислоты), перестройка генов и нарушение процессов транскрипции. В результате данных процессов снижается либо полностью блокируется синтезирование цепей глобина. Причины, которые могут привести к мутации генов:
- алкоголизм;
- вирусные заболевания;
- употребление наркотиков;
- ионизирующая радиация;
- химические мутагены, которые могут поступать в организм, например, при работе на вредных предприятиях;
- лекарственные препараты (Колхицин, статики и др).
Талассемия может наследоваться гомо- и гетерозиготно. В первом случае ребенок получает 2 дефектных гена (по одному от каждого родителя). Во втором, ген наследуется от одного родителя.
Симптомы
При гетерозиготной форме, заболевание может не проявляться клинически, либо иметь легкую форму с минимально выраженными симптомами. В данном случае основная жалоба – это повышенная утомляемость. По данным исследований выявляют незначительное увеличение селезенки и не выраженную гипохромную анемию.
При гомозиготной форме, заболевание проявляется яркими симптомами, характерными для талассемии. Самой распространенной является бета-форма, которая проявляется в первые годы жизни. Признаки бета-талассемии у детей:
- монголоидное лицо;
- четырехугольный (башенный) череп;
- увеличение размеров верхней челюсти;
- седловидная переносица;
- нарушение прикуса;
- увеличение объема печени, селезенки;
- землянисто-желтушные кожные покровы;
- отставание в росте;
- патологические переломы трубчатых костей.
У некоторых детей появляется желчнокаменная болезнь, язвы на коже ног, воспалительные процессы в крупных суставах. Избыток железа осложняет течение заболевания, приводя к фиброзу поджелудочной железы, циррозу печени, что влечет за собой сердечную недостаточность, сахарный диабет, кардиосклероз. Дети с талассемией склонны к инфекционным заболеваниям, вплоть до развития сепсиса. Из-за нарушения связывания гемоглобина с молекулами кислорода организм находится в состоянии гипоксии.
Гомозиготная альфа-талассемия связана с отсутствием альфа-цепей, поэтому данная форма патологии с жизнью несовместима и ведет к внутриутробной гибели.
Диагностика
Лечением и диагностикой заболевания занимаются врачи генетики и гематологи. При выявлении патологии важную роль играет семейный анамнез, из которого можно узнать о случаях гемоглобинопатии в роду. При осмотре ребенка обращают внимание на изменение цвета кожи, конституционные изменения (отставание в росте, изменение формы черепа, увеличение верхней челюсти).
Главные изменения при биохимическом и общем анализе крови, которые указывают на талассемию:
- уменьшение уровня Нb;
- гипохромная анемия;
- мишеневидные эритроциты;
- повышение количества железа;
- снижение цветового показателя;
- повышение содержания непрямого билирубина.
С помощью электрофореза гемоглобина определяют гемоглобиновые фракции, для выявления аномальных форм и снижения количества Нb А. На рентгенографии черепа при большой бета-талассемии обнаруживают феномен «волосатого черепа» (изменение в строении надкостницы в виде иголок). При рентгенографии костей выявляют очаги остеопороза (снижение количества костной ткани, которое ведет к хрупкости костей), исчерченность плоских, трубчатых костей.
По данным УЗИ – увеличение размеров печени, селезенки, камни в желчном пузыре. Для подтверждения заболевания проводят пункцию костного мозга, в котором обнаруживают повышенное количество эритробластов. С помощью молекулярно-генетических исследования определяют мутационные гены, которые приводят к нарушению синтезирования полипептидных цепей Нb.
При подозрении на аномалию гемоглобина проводят дифференциальную диагностику с заболеваниями, которые имеют схожую клиническую картину: серповидно-клеточная, железодефицитная, аутоиммунная гемолитическая анемия, наследственный микросфероцитоз. При планировании беременности, в семьях, где в роду были случаи талассемии необходимо генетическое консультирование, чтобы определить вероятность рождения больного ребенка.
Для определения аномалии при беременности выполняют амниоцентез, кордоцентез, биопсию хориона. При выявлении гомозиготных форм заболевания показано прерывание беременности.
Методы лечения
Лечебная тактика зависит от формы патологии и степени выраженности ее симптомов. При малой (гетерозиготной) бета-талассемии люди не нуждаются в лечении, так как они являются носителями поврежденного гена, и заболевание клинически не проявляется. При гомозиготной бета-талассемии лечение больного ребенка начинают с первых месяцев жизни. Консервативная терапия включает:
- Переливание крови.
- Выведение избыточного количества железа из организма, путем применения хелатирующих средств.
- Глюкокортикостероидные препараты для купирования приступов (кризов талассемии).
- Препараты фолиевой кислоты и другие витамины группы В.
Больные дети имеют склонность к развитию инфекционных заболеваний с быстро развивающимися осложнениями. Для снижения риска их развития проводят вакцинацию против пневмококковой инфекции.
Хирургическое лечение необходимо в тяжелых случаях – при прогрессирующих симптомах и осложнениях. При увеличении селезенки, камнях в желчном пузыре показано удаление данных органов. К оперативному лечению относят и трансплантацию костного мозга. Его берут у донора, клетки которого должны быть совместимы гистологически с клетками пациента.
Осложнения и профилактические меры
Из-за избыточного количества железа происходит его отложение в органах и тканях, что ведет к кардиосклерозу, циррозу печени, сахарному диабету, камням в желчном пузыре, сердечной недостаточности. На фоне талассемии люди часто подвергаются инфекционным заболеваниям, осложнения которых могут стать причиной летального исхода. Также к осложнениям относят и остеопороз, при котором кости становятся слабыми и хрупкими.
Первичные профилактические мероприятия заключаются в своевременном выявлении дефектного гена у супругов, которые планируют ребенка. Особенно в этом нуждаются пары, в роду которых была выявлена талассемия и супруги, которые имеют кровное родство. Если один или оба родителя имеют патологию, то в период беременности проводят обследование плода с помощью амницентеза или фетоскопии. Выбор способа зависит от возрастных особенностей, наличия сопутствующих заболеваний. С помощью данных методов получают клетки плода, которые подвергают медико-генетическому исследованию.
Большие формы талассемии имеют неблагоприятный прогноз, так дети умирают либо внутриутробно, либо в младенческом возрасте. При получении дефектного гена от одного родителя и наличии бессимптомной формы патологии прогноз благоприятный – качество жизни не страдает. Другие формы талассемии на фоне лечения, могут переходить в стадию ремиссии (затихания). Сдать кровь на определения дефектных генов, можно самостоятельно в частной клинике, например Инвитро. Расшифровка результатов занимает 7-10 дней.
источник