Серотониновые сети
Автор
Редактор
Нейромедиаторы осуществляют передачу сигналов между клетками в нервной системе. Разные группы нейронов объединяются в целые функциональные системы, которые «работают» на определенном веществе. В психиатрии и нейробиологии особое внимание уделяется серотонину — нейромедиатору, о котором и пойдет речь.
Сырное настроение
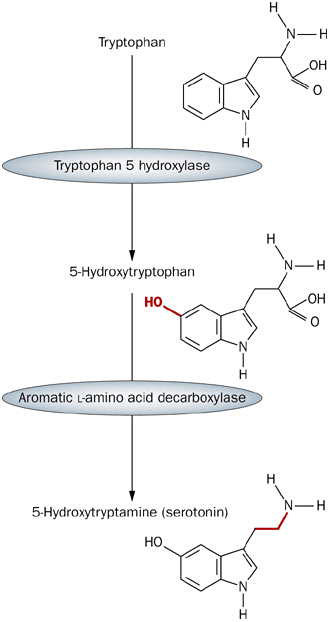
Рисунок 1. Две стадии синтеза серотонина из триптофана. Сначала к аминокислоте прикрепляется OH-группа, а затем отсоединяется карбоксильный радикал. (www.nature.com)
Ранее я уже писал о том, чем занимается дофамин в нашем мозге [1]. Сейчас речь пойдет о другом нейромедиаторе — серотонине. Как и в случае с дофамином, предшественником серотонина является аминокислота — триптофан. В состав триптофана входит ароматическое ядро индола, а само соединение синтезируется довольно сложным путем. Серотонин (5-гидрокситриптамин, 5-НТ) получается из триптофана всего за две реакции: сначала к индоловой части присоединяется гидроксильный радикал, а затем от получившейся молекулы отщепляется карбоксильная группа (рис. 1).
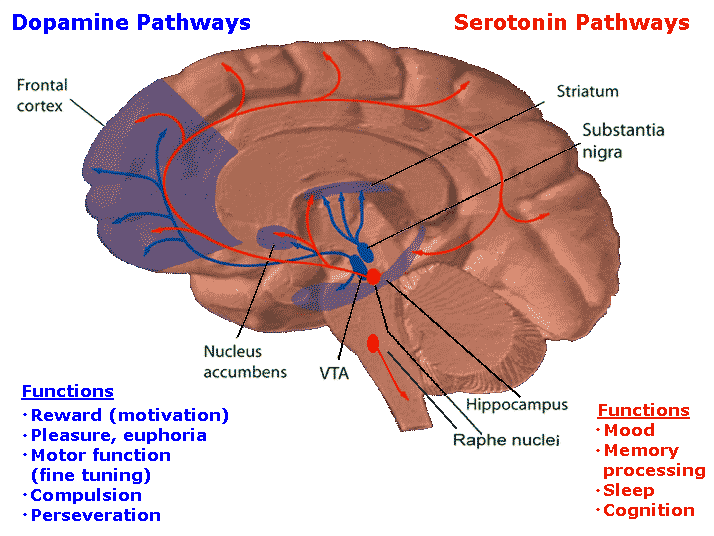
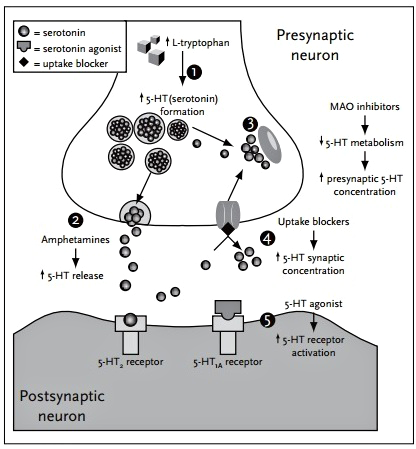
Схема распространения отростков серотониновых нейронов напоминает дофаминовую систему. Из глубоких отделов мозга — из комплекса скоплений нейронов, называемых ядра шва — сигналы разбегаются почти по всему органу (рис. 2). Уже на месте серотонин взаимодействует с рецепторами на постсинаптической мембране, осуществляя свои психофизиологические эффекты. Существует семь основных типов серотониновых рецепторов и множество их подтипов [2], но подробное описание их роли займет слишком много места.
Рисунок 2. Серотониновые и дофаминовые пути в головном мозге человека. Дофаминовые волокна из глубоких отделов мозга распространяются в подкорковые отделы и в лобную долю. Отростки серотониновых нейронов распространяются шире и влияют на большее количество функций. Рисунок из Википедии (англ.).
Лучше обратить внимание на то, как содержание триптофана, предшественника серотонина, может повлиять на наше поведение. Логично предположить, что повышение количества триптофана в пище приведет к тому, что увеличится и уровень серотонина. При депрессии содержание серотонина в центральной нервной системе снижается. Можно представить такой эксперимент: из рациона человека исключается триптофан. Вследствие этого страдает синтез серотонина, и мы наблюдаем снижение настроения — типичный симптом депрессии. На практике это работает немного по-другому. При уменьшении поступления триптофана с пищей снижение настроения отмечается только у тех людей, которые раньше болели депрессией [3]. Отказ от триптофана не оказывал значимого влияния на испытуемых без депрессивных эпизодов в прошлом. По всей видимости, это связано с изменёнными путями метаболизма серотонина у пациентов с депрессивными расстройствами, которых нет у здоровых людей.
Интересно, что если уровень триптофана в пище будет высоким, это может привести к щедрости. В исследовании голландских психологов [4] была выявлена именно такая связь. Испытуемые, принявшие большую дозу триптофана, жертвовали больше денег, чем те участники эксперимента, которые ее не получили. Сами исследователи объясняют повышенную щедрость связью между серотониновой и окситоциновой системами в головном мозге. Неспецифическое повышение интенсивности сигнала в серотониновой системе приводит к увеличению активности всех связанных с ней структур. Окситоциновые нейроны не становятся исключением, и в мозге появляется больше окситоцина. Такое повышение приводит к тому, что мозг человека становится более предрасположенным к выбору в пользу других людей. Кстати, лидером по содержанию триптофана среди пищевых продуктов является сыр, и было бы интересно проследить взаимосвязь между потреблением сыра и щедростью у разных народов.
Нейромедиатор контроля
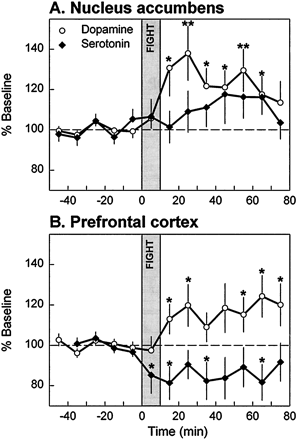
Рисунок 3. Изменение содержания нейромедиаторов у крыс в состоянии агрессии. Во время драки (серая вертикальная полоса) и после неё повышается содержание дофамина в добавочном ядре (А), регулирующем поведение и мотивацию, и снижается высвобождение серотонина в лобных отделах коры (B). Звездочки указывают на существенные различия с базовыми уровнями нейромедиаторов. Рисунок из [5].
Как уже говорилось, серотонин распространяется из продолговатого мозга, из ядер шва. Существенная разница с дофаминовой системой заключается в более широком охвате структур головного мозга серотониновыми волокнами. Такой охват позволяет серотонину влиять на процессы памяти и когнитивные способности: темп и качество мышления. При депрессии снижение интенсивности серотониновой передачи приводит к ухудшению сообразительности и замедлению мышления.
Кроме влияния на интеллект серотонин оказывает серьезное воздействие на агрессивное поведение. Например, у крыс сравнивалось содержание дофамина и серотонина в подкорковых структурах и лобной доле при драках [5]. Ученые выяснили, что агрессивное поведение животных связано со снижением уровня серотонина в лобных отделах коры, отвечающих за планирование и контроль поведения (рис. 3). У людей также показана связь между пониженным уровнем серотонина в лобных отделах коры и агрессивным поведением, но только импульсивным, возникающим внезапно [6].
Серотонин снижает активность нейронов префронтальной коры не прямым воздействием на них, а через тормозные нейроны, выделяющие гамма-аминомасляную кислоту (ГАМК). Нейромедиатор попадает на рецепторы, расположенные на теле и отростках ГАМК-ергических нейронов, блокируя или запуская передачу сигнала [7]. Примечательно, что при уменьшении активности отдельных нейронов под воздействием серотонина увеличивается упорядоченная активность нейронных систем, то есть серотонин упорядочивает совместную работу нейронов, не давая им перебивать друг друга в многоголосой беседе.
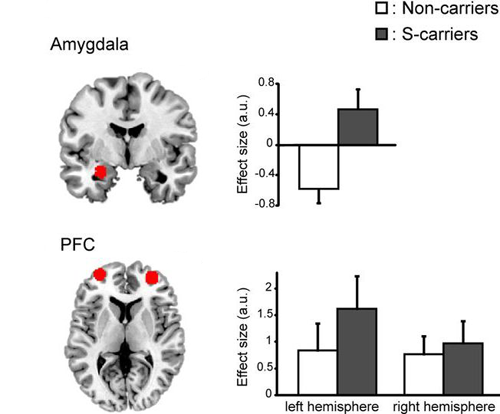
В вопросах влияния серотонина на личность стоит обратить внимание на один из генов серотониновой системы — ген белка-транспортёра серотонина (5-HTT, SERT). Существуют два варианта промоторной последовательности этого гена (serotonin transporter linked polymorphic region, 5-HTTLPR), различающиеся длиной, причем короткий вариант выполняет свою работу хуже, чем длинный. При исследовании влияния полиморфизма 5-HTTLPR на особенности социальной жизни оказалось, что обладатели короткого аллеля более склонны к тревожным реакциям при социальном взаимодействии [8]. Носители короткого варианта в гомозиготном и гетерозиготном состоянии проявляли повышенную чувствительность к эмоциональным стимулам и хуже контролировали своё поведение. В исследовании, опубликованном в 2013-м году в The Journal of Neuroscience [9], было показано, что у обладателей короткого аллеля 5-HTTLPR префронтальная кора хуже контролирует работу миндалины — центра эмоционального реагирования (рис. 4), который чувствителен и к другим «эмоциональным» аллелям, например, к полиморфизму гена моноаминоксидазы-А [10]. Выяснилось, что в течение жизни на активность 5-HTT может оказывать влияние опыт негативного взаимодействия с окружающими, например, жестокое обращение в детстве. Такие события ухудшают и без того слабую работу белка-транспортёра, приводя к нарушениям в работе головного мозга, вроде описанных выше.
Рисунок 4. Возбудимость миндалины (сверху) и передней префронтальной коры (снизу) в зависимости от полиморфизма промотора гена транспортёра серотонина. У обладателей короткого (S-, темные столбцы) варианта 5-HTTLPR активация миндалины выше, чем у носителей длинного аллеля (белые столбцы). На нейробиологическом уровне это значит, что мозг «захлестывают» эмоции. Чтобы справиться с этим информационным потоком, наблюдаемого незначительного повышения активности префронтальной коры в левом и правом полушариях не достаточно. Рисунок из [9].
Рискованные лекарства
Учитывая вовлеченность серотонина в психические процессы, ряд лекарств, которыми пользуются психиатры и психотерапевты, прицельно воздействует на серотониновые системы. Самым известным классом подобных препаратов являются антидепрессанты [11]. Среди антидепрессантов стоит отметить селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) и селективные ингибиторы обратного захвата серотонина (СИОЗС).
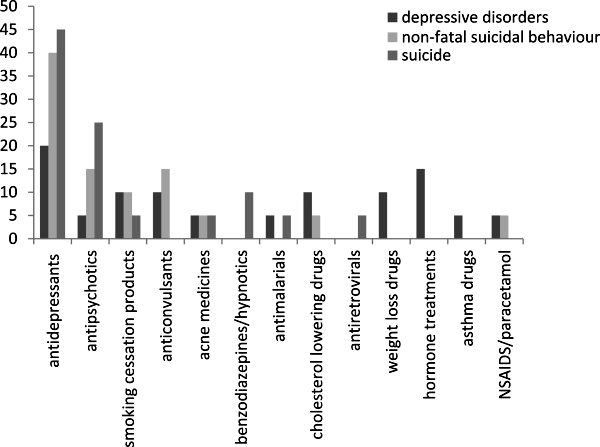
Рисунок 5. Антидепрессанты — лидеры по поведенческим побочным эффектам [12].
Принцип работы этих лекарств довольно прост. Под воздействием электрического сигнала из одного нейрона в синаптическую щель начинает выделяться серотонин. Связавшись с рецептором на поверхности другого нейрона, он удаляется из синапса при помощи специального фермента. При применении СИОЗС нарушение деятельности фермента, осуществляющего обратный захват серотонина, приводит к увеличению силы сигнала в серотониновой системе мозга. К классу СИОЗС относится всем известный прозак (флуоксетин). Другая группа препаратов — СИОЗСН — подавляет обратный захват как серотонина, так и норадреналина; среди них широко применяются венлафаксин и дулоксетин. На похожем принципе — подавлении обратного захвата нейромедиаторов — основана работа классического антидепрессанта амитриптилина, который «берёт еще шире»: не только тормозит захват серотонина и норадреналина, но и меняет активность транспортёров этих нейромедиаторов.
Однако с СИОЗС возник ряд проблем. В британском исследовании, которое объединило данные по нежелательным эффектам лекарств за 13 лет, эта группа антидепрессантов проявила себя не с самой лучшей стороны [12]. Среди всех препаратов, которые вызывали при приеме депрессию, пароксетин занял третье место. В случае суицидальных попыток, не приведших к смерти, чаще всего фигурировали СИОЗС пароксетин (1-е место), циталопрам (3-е место) и флуоксетин (4-е место). Если же смотреть по завершенным самоубийствам, то 2-е, 3-е и 4-е места заняли циталопрам, флуоксетин и пароксетин соответственно. Чаще всего именно антидепрессанты были связаны со всеми перечисленными нежелательными эффектами (рис. 5).
С одной стороны, эта информация выглядит пугающе и непонятно: как могут антидепрессанты провоцировать самоубийства? С другой стороны, у этого феномена могут быть два объяснения. Антидепрессанты назначаются в случае депрессии, а при депрессии часто бывают суицидальные мысли и намерения, поэтому нет ничего удивительного, что у человека с депрессией, даже принимающего препараты, может случиться суицидальный эпизод. Другое объяснение лежит в принципе действия группы СИОЗС: они напрямую вмешиваются в нейрометаболизм. Мы до сих пор не очень хорошо разбираемся в работе головного мозга и не можем выделить точные критерии для применения того или иного препарата. По этим причинам назначение СИОЗС может привести к нарушению работы головного мозга, усугублению проблем с нейромедиаторами. Но даже несмотря на это, в подавляющем большинстве случаев антидепрессанты работают должным образом, а описанные побочные эффекты остаются весьма редкими.
Рисунок 6. Механизм развития серотонинового синдрома. Применение СИОЗС приводит к увеличению концентрации серотонина в синаптической щели. ИМАО вызывают повышение количества этого нейромедиатора в пресинаптическом нервном окончании. Вместе эти два фактора обеспечивают избыток серотонина в нервных путях. Рисунок из [13].
Другим серьезным побочным эффектом, возникающим при применении серотонинергических препаратов, является серотониновый синдром. Серотониновый синдром — это состояние организма, при котором отмечается усиленное воздействие этого нейромедиатора на организм, чрезмерная активация серотонинергических структур головного мозга. Такое происходит, например, при одновременном назначении двух типов антидепрессантов — СИОЗС и ингибитора моноаминоксидазы (ИМАО). Если СИОЗС препятствуют удалению серотонина из синаптической щели, то ИМАО подавляют разрушение серотонина в пресинаптическом окончании. Последствием этих процессов будет повышенное содержание серотонина в синапсе и увеличение интенсивности сигналов в серотонинергической системе (рис. 6).
Кроме лекарственных средств серотониновый синдром может вызываться приемом экстази. Клинически это состояние проявляется следующим набором симптомов: у пациента повышается температура, он беспокоен или находится без сознания, у него могут участиться сердцебиение и дыхание, появиться одышка. Довершают картину болезни колебания артериального давления, диарея и беспорядочные мышечные сокращения. В случае диагностированного серотонинового синдрома отменяются все серотонинергические препараты; пациенту проводится дезинтоксикация [13]. Как и в случае с суицидальным поведением, серотониновый синдром встречается крайне редко, поэтому не стоит бояться их при лечении антидепрессантами группы СИОЗС.
Исследование серотониновой системы человеческого мозга еще раз возвращает нас к тому, насколько мы зависим от биологических, а не только социальных, факторов. Количество съедаемого сыра, гены, переданные нам от родителей, назначенные лекарства — всё это меняет метаболизм в мозге, а значит, меняет и нас. Конечно, можно сказать, что есть общение с другими людьми, различия в индивидуальном опыте, то есть чисто социальные моменты, но не надо забывать, что социальная составляющая нашей личности реализуется всё теми же биологическими — и доступными для исследования — механизмами нашей психики.
источник
Метаболизм (анаболизм и катаболизм) серотонина
Иммунная система, в том числе и вилочковая железа (тимус) производит большое количество гормонов, которые можно подразделить на цитокины или лимфокины и тимические (или тимусные) гормоны — тимопоэтины, регулирующие процессы роста, созревания и дифференцировки Т-клеток и функциональную активность зрелых клеток иммунной системы. К цитокинам, секретируемым иммунокомпетентными клетками, относятся: гама-интерферон, интерлейкины (1—7 и 9—12), фактор некроза опухолей, гранулоцитарный колониестимулирующий фактор, гранулоцитомакрофагальный колониестимулирующий фактор, макрофагальный колониестимулирующий фактор, лейкемический ингибиторный фактор, онкостатин М, фактор стволовых клеток и другие [1] . С возрастом тимус деградирует, заменяясь соединительнотканным образованием.
Диффузная эндокринная система
В диффузной эндокринной системе эндокринные клетки не сконцентрированы, а рассеяны.
Некоторые эндокринные функции выполняют печень (секреция соматомедина, инсулиноподобных факторов роста и др.), почки (секреция эритропоэтина, медуллинов и др.), желудок (секреция гастрина), кишечник (секреция вазоактивного интестинального пептида и др.), селезёнка (секреция спленинов) и др. Эндокринные клетки содержатся во всём организме человека.
Выделено и описано более 30 гормонов, которые секретируются в кровяное русло клетками или скоплениями клеток, расположенными в тканях желудочно-кишечного тракта. Эндокринные клетки желудочно-кишечного тракта синтезируют гастрин, гастринсвязывающий пептид, секретин, холецистокинин, соматостатин, вазоактивный интестинальный полипептид (ВИП), вещество P, мотилин, галанин, пептиды гена глюкагона (глицентин, оксинтомодулин, глюкагоноподобный пептид 1 и 2), нейротензин,нейромедин N, пептид YY, панкреатический полипептид, нейропептид Y, хромогранины (хромогранин A и относящиеся к нему пептид GAWK и секретогранин II).
Регуляция эндокринной системы
Эндокринный контроль можно рассматривать как цепь регуляторных эффектов, в которой результат действия гормона прямо или косвенно влияет на элемент, определяющий содержание доступного гормона.
· Взаимодействие происходит, как правило, по принципу отрицательной обратной связи: при воздействии гормона на клетки-мишени их ответ, влияя на источник секреции гормона, вызывает подавление секреции.
· Положительная обратная связь, при которой секреция усиливается, встречается крайне редко.
· Эндокринная система также регулируется посредством нервной и иммунной систем.
Эндокринные заболевания — это класс заболеваний, которые возникают в результате расстройства одной или нескольких эндокринных желёз. В основе эндокринных заболеваний лежат гиперфункция, гипофункция или дисфункция желёз внутренней секреции.
Апудо́мы — опухоли, исходящие из клеточных элементов, расположенных в различных органах и тканях (преимущественно островковые (инкреторные) клетки поджелудочной железы, клетки других отделов ЖКТ, С-клетки щитовидной железы), продуцирующих полипептидные гормоны. В настоящее время описаны следующие виды апудом [2] :
Синдром Випома
Основная статья: ВИПома
ВИПо́ма (синдром Вернера-Моррисона, панкреатическая холера, синдром водной диареи-гипокалиемии-ахлоргидрии) — характеризуется наличием водной диареи и гипокалиемии в результате гиперплазии островковых клеток или опухоли, часто злокачественной, исходящей из островковых клеток поджелудочной железы (чаще тела и хвоста), которые секретируют вазоактивный интестинальный полипептид (ВИП). В редких случаях ВИПома может приходиться на ганглионейробластомы, которые локализуются в ретроперитонеальном пространстве, лёгких, печени, тонкой кишке и надпочечниках, встречаются в детском возрасте и, как правило, доброкачественные. Размер панкреатических ВИПом 1…6 см. В 60 % случаев злокачественных новообразований на момент диагностики имеются метастазы [3] . Заболеваемость ВИПомой очень мала (1 случай в год на 10 млн человек) или 2 % от всех эндокринных опухолей желудочно-кишечного тракта. В половине случаев опухоль злокачественная. Прогноз чаще неблагоприятный [4] .
При гиперплазии G-клеток образуется гастрино́ма — доброкачественная или злокачественная опухоль, локализующаяся в поджелудочной железе, двенадцатиперстной или тощей кишке, или даже в перипанкреатических лимфатических узлах, в воротах селезёнки или стенке желудка. Эта опухоль вырабатывает большее количество гастрина, возникает гипергастринимия, которая, через механизм стимуляции париетальных клеток, является причиной чрезмерной продукции соляной кислоты и пепсина. В нормальной ситуации G-клетки под воздействием соляной кислоты тормозят выработку гастрина, но на G-клетки гастрино́м фактор кислотности не влияет. В результате развиваются множественные пептические язвы желудка, двенадцатиперстной или тощей кишки. Секреция гастрина гастриномами особенно резко усиливается после приёма пищи.
Клиническое проявление гипергастринимии — синдром Золлингера — Эллисона (1-го типа) [5] .
Глюкагонома
Глюкагоно́ма — опухоль, чаще злокачественная, исходящая из альфа-клеток панкреатических островков. Характеризуется мигрирующим эрозивным дерматозом, ангулярным апапахейлитом, стоматитом, глосситом, гипергликемией, нормохромной анемией. Растёт медленно, метастазирует в печень. Встречается 1 случай на 20 млн в возрасте от 48 до 70 лет, чаще у женщин [2] .
Карциноид — злокачественная опухоль, обычно возникающая в желудочно-кишечном тракте, которая вырабатывает несколько веществ, обладающих гормоноподобным действием
ППо́ма — опухоль поджелудочной железы, секретирующая панкреатический полипептид (ПП). Клинические проявления практически отсутствуют. Чаще диагностируется после метастазирования в печень [2] . Лечение: оперативное, химиотерапия и симптоматическое. Прогноз зависит от срока начала лечения.
Соматостатинома
Сома́тостатино́ма — злокачественная медленно растущая опухоль, характеризуется повышением уровня соматостатина. Это редкое заболевание, встречается у лиц старше 45 лет — 1 случай на 40 млн [2] .
· соматостатиному из дельта-клеток поджелудочной железы и
· апудому, секретирующую соматостатин — опухоль двенадцатиперстной кишки.
Диагноз на основании клиники и повышения уровня соматостатина в крови. Лечение оперативное, химиотерапия и симптоматическое. Прогноз зависит от своевременности лечения.
| Структура | Название | Сокращение | Место синтеза | Механизм действия |
| Триптамин | мелатонин (N-ацетил-5-метокситриптамин) | эпифиз | ||
| Триптамин | серотонин | 5-HT | энтерохромаффинные клетки | |
| производное тирозина | тироксин | T4 | щитовидная железа | ядерный рецептор |
| производное тирозина | трийодтиронин | T3 | щитовидная железа | ядерный рецептор |
| производное тирозина(катехоламин) | адреналин (эпинефрин) | мозговой слой надпочечников | ||
| производное тирозина(катехоламин) | норадреналин (норэпинефрин) | мозговой слой надпочечников | ||
| производное тирозина(катехоламин) | дофамин | DA | гипоталамус | |
| пептид | антимюллеров гормон (ингибирующее вещество Мюллера) | АМГ | клетки Сертоли | |
| пептид | адипонектин | жировая ткань | ||
| пептид | адренокортикотропный гормон (кортикотропин) | АКТГ | передняя доля гипофиза | цАМФ |
| пептид | ангиотензин, ангиотензиноген | печень | IP3 | |
| пептид | антидиуретический гормон (вазопрессин) | АДГ | гипоталамус (накапливается в задней доле гипофиза) | |
| пептид | предсердный натрийуретический пептид | АНФ | Секреторные кардиомиоциты правого предсердия сердца | цГМФ |
| пептид | глюкозозависимый инсулинотропный полипептид | ГИП | K-клетки двенадцатиперстной итощей кишок | |
| пептид | кальцитонин | щитовидная железа | цАМФ | |
| пептид | кортикотропин-высвобождающий гормон | АКГГ | гипоталамус | цАМФ |
| пептид | холецистокинин (панкреозимин) | CCK | I-клетки двенадцатиперстной и тощейкишок | |
| пептид | эритропоэтин | почки | ||
| пептид | фолликулостимулирующий гормон | ФСГ | передняя доля гипофиза | цАМФ |
| пептид | гастрин | G-клетки желудка | ||
| пептид | грелин (гормон голода) | Эпсилон-клетки панкреатических островков, гипоталамус | ||
| пептид | глюкагон (антагонист инсулина) | альфа-клетки панкреатических островков | цАМФ | |
| пептид | гонадотропин-высвобождающий гормон (люлиберин) | GnRH | гипоталамус | IP3 |
| пептид | соматотропин-высвобождающий гормон («гормон роста»-высвобождающий гормон, соматокринин) | GHRH | передняя доля гипофиза | IP3 |
| пептид | человеческий хорионический гонадотропин | hCG, ХГЧ | плацента | цАМФ |
| пептид | плацентарный лактоген | ПЛ, HPL | плацента | |
| пептид | соматотропный гормон (гормон роста) | GH or hGH | передняя доля гипофиза | |
| пептид | ингибин | |||
| пептид | инсулин | бета-клетки панкреатических островков | Тирозинкиназа,IP3 | |
| пептид | инсулиноподобный фактор роста (соматомедин) | ИФР, IGF | Тирозинкиназа | |
| пептид | лептин (гормон насыщения) | жировая ткань | ||
| пептид | лютеинизирующий гормон | ЛГ, LH | передняя доля гипофиза | цАМФ |
| пептид | меланоцитстимулирующий гормон | МСГ | передняя доля гипофиза | цАМФ |
| пептид | нейропептид Y | |||
| пептид | окситоцин | гипоталамус (накапливается в задней доле гипофиза) | IP3 | |
| пептид | панкреатический полипептид | PP | PP-клетки панкреатических островков | |
| пептид | паратиреоидный гормон (паратгормон) | PTH | паращитовидная железа | цАМФ |
| пептид | пролактин | передняя доля гипофиза | ||
| пептид | релаксин | |||
| пептид | секретин | SCT | S-клетки слизистой оболочки тонкой кишки | |
| пептид | соматостатин | SRIF | дельта-клетки панкреатических островков, гипоталамус | |
| пептид | тромбопоэтин | печень, почки | ||
| пептид | тироид-стимулирующий гормон | передняя доля гипофиза | цАМФ | |
| пептид | тиреолиберин | TRH | гипоталамус | IP3 |
| Глюкокортикоид | кортизол | кора надпочечников | прямой | |
| минералокортикоид | альдостерон | кора надпочечников | прямой | |
| половой стероид (андроген) | тестостерон | яички | ядерный рецептор | |
| половой стероид (андроген) | дегидроэпиандростерон | ДГЭА | кора надпочечников | ядерный рецептор |
| половой стероид (андроген) | андростендиол | яичники, яички | прямой | |
| половой стероид (андроген) | дигидротестостерон | множественное | прямой | |
| половой стероид (эстроген) | эстрадиол | фолликулярный аппарат яичников,яички | прямой | |
| половой стероид (прогестин) | прогестерон | жёлтое тело яичников | ядерный рецептор | |
| Стерин | кальцитриол | почки | прямой | |
| Эйкозаноид | простагландины | семенная жидкость | ||
| Эйкозаноид | лейкотриены | белые кровяные клетки | ||
| Эйкозаноид | простациклин | эндотелий | ||
| Эйкозаноид | тромбоксан | тромбоциты |
Мелатонин — основной гормон эпифиза, регулятор суточных ритмов.
Может приниматься в таблетках для облегчения засыпания, с целью корректировки «внутренних часов» при длительных путешествиях (см. джетлаг).
Гормон мелатонин был открыт в 1958 году А. Б. Лернером. Изменения концентрации мелатонина имеют заметный суточный ритм в шишковидном теле и в крови, как правило, с высоким уровнем гормона в течение ночи и низким уровнем в течение дня. Максимальные значения концентрации мелатонина в крови человека наблюдаются между полуночью и 5 часами утра поместному солнечному времени. Вырабатывается основными секреторными клетками эпифиза — пинеалоцитами.
Время биологического полураспада мелатонина равно 45 минутам. Это означает, что для исследовательских целей образцы крови должны быть собраны через короткие промежутки времени для того, чтобы определить период в продукции мелатонина. Кроме того, нарушение сна пациента в течение ночи с целью сбора образцов может повлиять на уровень мелатонина в крови. Этих проблем можно избежать, если определять уровни метаболитов мелатонина: мелатонин сульфата (6-сульфатоксимелатонина) и 6-гидроксиглюкуронида в моче. 80—90 % мелатонина секретируется в мочу в виде мелатонин сульфата. Концентрация мелатонин сульфата в моче хорошо коррелирует с общим уровнем мелатонина в крови в течение периода сбора образцов.
Синтезированный в эпифизе мелатонин поступает в кровь и спинномозговую жидкость — ликвор, пройдя через которую, накапливается в гипоталамусе. Помимо крови и цереброспинальной жидкости, мелатонин обнаружен в моче, слюне,амниотической жидкости.
Мелатонин повсеместно встречается в животном мире. Есть мелатонин как у растений, так и у простейших.
Синтез мелатонина (а также серотонина, ниацина) из триптофана
В организме человека мелатонин синтезируется из аминокислоты триптофана, которая участвует в синтезе нейромедиатора(нейропередатчика) серотонина, а он в свою очередь под воздействием фермента N-ацетилтрансферазы превращается в мелатонин. Показано, что мелатонин является индольным производным серотонина и синтезируется ночью ферментами N-ацетилтрансферазой и гидроксииндол-О-метилтрансферазой. У взрослого человека за сутки синтезируется около 30 мкг [источник не указан 451 день] мелатонина, его концентрация в сыворотке крови ночью в 30 раз больше, чем днем, причём максимум концентрации в среднем по множеству наблюдений приходится приблизительно на 2 часа ночи [2] [3] по местному солнечному времени. Мелатонин транспортируется сывороточным альбумином, после освобождения от альбумина связывается со специфическимирецепторами на мембране клеток-мишеней, проникает в ядро и там осуществляет своё действие. Мелатонин быстро гидролизуется в печени и экскретируется с мочой, основным метаболитом является 6-гидроксимелатонин-сульфат (6-СОМТ), содержание которого позволяет косвенно судить о продукции мелатонина эпифизом.
Секреция мелатонина подчинена суточному ритму, определяющему, в свою очередь, ритмичность гонадотропных эффектов и половой функции. Синтез и секреция мелатонина зависят от освещённости — избыток света понижает его образование, а снижение освещённости увеличивает синтез и секрецию гормона. У человека на ночные часы приходится 70 % суточной продукции мелатонина.
Мелатонин — редкий пример гормона, у которого имеются как мембранные, так и ядерные рецепторы. У млекопитающих имеется два мембранных рецептора мелатонина — MTNR1A (MT1), экспрессирующийся в основном на клетках передней доли гипофиза и супрахиазменных ядер гипоталамуса, но также присутствующий во многих периферических органах, и MTNR1B (MT2), экспрессирующийся в некоторых других участках мозга, в сетчатке и в лёгких. У птиц, амфибий и рыб имеется третий рецептор — MTNR1С (MT3), который у млекопитающих пока не клонирован. Рецепторы мелатонина относятся к семейству рецепторов, связанных с G-белками, и действуют через Gαi-белок, снижая уровень цАМФ.
Средство от бессонницы рамелтеон (ramelteon), выпускаемое в США под торговым названием Rozerem, связывается с обоими типами рецепторов мелатонина. С этими же рецепторами связывается антидепрессант агомелатин, зарегистрированный в России под торговым названием Вальдоксан.
Недавно открытые ядерные рецепторы мелатонина относятся к подсемейству RZR/ROR ретиноидных рецепторов. Видимо, через них опосредуются многие иммуностимулирующие и противоопухолевые эффекты мелатонина.
Регулирует деятельность эндокринной системы, кровяное давление, периодичность сна
· Регулирует сезонную ритмику у многих животных
· Замедляет процессы старения
· Усиливает эффективность функционирования иммунной системы
· Обладает антиоксидантными свойствами
· Влияет на процессы адаптации при смене часовых поясов
Кроме того, мелатонин участвует в регуляции
· функций пищеварительного тракта,
· работы клеток головного мозга.
Серотони́н, 5-гидрокситриптамин, 5-НТ — один из основных нейромедиаторов. По химическому строению серотонин относится к биогенным аминам, классу триптаминов. Серотонин часто называют «гормоном хорошего настроения» и «гормоном счастья». [1]
В 1935 году итальянским фармакологом Витторио Эрспамером впервые было экстрагировано вещество из слизистой ЖКТ, сокращающее гладкую мускулатуру. Некоторые считали, что это был всего лишь адреналин, но только через два года первооткрывателю удалось доказать, что этим веществом оказался ранее неизвестный амин. Эрспамер назвал полученное соединение «энтерамином» [2] . В 1948 году Морис Раппорт, Арда Грин и Ирвин Пейдж в Кливлендской клинике обнаружили сосудосуживающее вещество в сыворотке крови, которое назвали «серотонином». Структура данного вещества, предложенная Морисом Раппортом, в 1951 году была подтверждена химическим синтезом. В 1952 году было доказано, что энтерамин и серотонин — одно и то же вещество [3] . В 1953 году нейрофизиологам Ирвину Пейджу и Бетти Твэрег удалось обнаружить серотонин в головном мозге [4] .
После открытия серотонина началось изучение его рецепторов. В 1957 Джон Гаддум провёл ряд исследований, по итогам которых выяснилось, что серотониновые рецепторы неоднородны: способность серотонина сокращать гладкие мышцыблокировалась диэтиламидом Д-лизергиновой кислоты (ЛСД — мощный галлюциноген ипсихотропный препарат вёл себя как агонист серотонина в периферических тканях), а свойство возбуждать вегетативные нервные узлы предотвращалось морфином. Соответствующие рецепторы были названы «Д»- и «М»-серотониновыми рецепторами. В 90-х годах XX-века с помощью методов молекулярной биологииудалось выяснить, что существуют, по крайней мере, 14 видов серотониновых рецепторов, которые отвечают за разнообразные функции серотонина.
Серотонин образуется из аминокислоты триптофана путём её последовательного 5-гидроксилирования ферментом 5-триптофангидроксилазой (в результате чего получается 5-гидрокситриптофан, 5-ГТ) и затем декарбоксилирования получившегося гидрокситриптофана ферментом триптофандекарбоксилазой. 5-триптофангидроксилаза синтезируется только в соме серотонинергических нейронов, гидроксилирование происходит в присутствии ионов железа и кофактораптеридина.
Рецепторы серотонина
Рецепторы серотонина представлены как метаботропными, так и ионотропными. Всего насчитывается семь типов таких рецепторов, 5-HT 1-7, причём 5-HT3-рецептор — ионотропный, остальные — метаботропные, семидоменные, связанные с G-белками. Установлено сходство метаботропных 5-HT рецепторов с рецепторами норадреналина.
5-HT1 тип, насчитывающий несколько подтипов: 5-HT1A, 5-HT1B, 5-HT1D, 5-HT1E, которые могут быть как пре-, так и постсинаптическими, подавляет аденилатциклазу; 5-HT4 и 5-HT7 — стимулируют; 5-HT2, насчитывающий несколько подтипов: 5-HT2А, 5-HT2B, 5-HT2C, которые могут быть только постсинаптическими, активирует инозитолтрифосфат. 5-HT5также подавляет аденилатциклазу [5] .
Для некоторых типов рецепторов обнаружены эндогенные лиганды, помимо серотонина. Это, например, 5HT-модулин (Leu-Ser-Ala-Leu), эндогенный лиганд 1B и 1D пресинаптических рецепторов, индуктор тревожности и стресса.
Структура серотонина имеет сходство со структурой психоактивного вещества ЛСД. ЛСД действует как агонист некоторых 5-HT рецепторов и ингибирует обратный захват серотонина, увеличивая его содержание.
Серотонин и норадреналин
Существует определенное сходство в строении клеточных рецепторов к серотонину и норадреналину, подобие их транспортных клеточных систем. Известно также, что норадреналин ингибирует выброс серотонина. На их связи основано действие антидепрессанта миртазапина, который, блокируя альфа-2 рецепторы норадреналина, по принципу отрицательной обратной связи повышает содержание в синаптической щели и норадреналина, и серотонина (так как его ингибирование также тормозится) до нормы.
Физиологическая роль
Физиологические функции серотонина чрезвычайно многообразны. Серотонин «руководит» очень многими функциями в организме. При снижении серотонина повышается чувствительность болевой системы организма, то есть даже самое слабое раздражение отзывается сильной болью.
Серотонин как нейромедиатор
Серотонин играет роль нейромедиатора в ЦНС. Серотонинергические нейроны группируются в стволе мозга: в варолиевом мосту и ядрах шва. От моста идут нисходящие проекции в спинной мозг, нейроны ядер шва дают восходящие проекции к мозжечку, лимбической системе, базальным ганглиям, коре. При этом нейроны дорсального и медиального ядер шва дают аксоны, различающиеся морфологически, электрофизиологически, мишенями иннервации и чувствительностью к некоторым нейротоксичным агентам, например, метамфетамину.
«Круговорот» серотонина
Синтезированный нейроном серотонин закачивается в везикулы. Этот процесс является протон-сопряженным транспортом. В везикулу с помощью протон-зависимой АТФазы закачиваются ионы H + . При выходе протонов по градиенту в везикулу поступают молекулы серотонина.
Далее, в ответ на деполяризацию терминали, серотонин выводится в синаптическую щель. Часть его участвует в передаче нервного импульса, воздействуя на клеточные рецепторы постсинаптической мембраны, а часть возвращается в пресинаптический нейрон с помощью обратного захвата. Ауторегуляция выхода серотонина обеспечивается путём активации пресинаптических 5-НТ рецепторов, запускающих каскад реакций, которые регулируют вход ионов кальция внутрь пресинаптической терминали. Ионы кальция, в свою очередь, активируют фосфорилирование фермента 5-триптофангидроксилазы, обеспечивающей превращение триптофана в серотонин, что приводит к усилению синтеза серотонина.
Обратный захват производится транспортером серотонина, двенадцатидоменным белком, производящим натрий-калий-сопряженный транспорт. Вернувшийся в клетку медиатор расщепляется с помощью моноаминооксидазы (МАО) до 5-гидроксилиндолилуксусной кислоты.
Химизм транспортных систем серотонина также подобен таковым норадреналина.
Функции серотонина
Серотонин облегчает двигательную активность, благодаря усилению секреции субстанции Р в окончаниях сенсорных нейронов путём воздействия на ионотропные и метаботропные рецепторы.
Серотонин наряду с дофамином играет важную роль в механизмах гипоталамической регуляции гормональной функции гипофиза. Стимуляция серотонинергических путей, связывающих гипоталамус с гипофизом, вызывает увеличение секреции пролактина и некоторых других гормонов передней доли гипофиза — действие, противоположное эффектам стимуляции дофаминергических путей.
Серотонин также участвует в регуляции сосудистого тонуса.
Серотониновый синдром
Избыток серотонина может быть потенциально опасен, вызывая последствия, известные как серотониновый синдром. Такая критическая концентрация серотонина зачастую является следствием параллельного применения антидепрессантов классов ингибиторов моноаминооксидазы и селективных ингибиторов обратного захвата серотонина [6] .
Серотонин как гормон
Серотонин играет важную роль в процессах свёртывания крови. Тромбоциты крови содержат значительные количества серотонина и обладают способностью захватывать и накапливать серотонин из плазмы крови. Серотонин повышает функциональную активность тромбоцитов и их склонность к агрегации и образованию тромбов. Стимулируя специфические серотониновые рецепторы в печени, серотонин вызывает увеличение синтеза печенью факторов свёртывания крови. Выделение серотонина из повреждённых тканей является одним из механизмов обеспечения свёртывания крови по месту повреждения.
Серотонин участвует в процессах аллергии и воспаления. Он повышает проницаемость сосудов, усиливает хемотаксис и миграцию лейкоцитов в очаг воспаления, увеличивает содержание эозинофилов в крови, усиливает дегрануляцию тучных клеток и высвобождение других медиаторов аллергии и воспаления. Местное (например, внутримышечное) введение экзогенного серотонина вызывает сильную боль в месте введения. Предположительно серотонин наряду с гистамином и простагландинами, раздражая рецепторы в тканях, играет роль в возникновении болевой импульсации из места повреждения или воспаления.
Также большое количество серотонина производится в кишечнике. Серотонин играет важную роль в регуляции моторики и секреции в желудочно-кишечном тракте, усиливая его перистальтику и секреторную активность. Кроме того, серотонин играет роль фактора роста для некоторых видов симбиотических микроорганизмов, усиливает бактериальный метаболизм в толстой кишке. Сами бактерии толстой кишки также вносят некоторый вклад в секрецию серотонина кишечником, поскольку многие виды симбиотических бактерий обладают способностью декарбоксилировать триптофан. При дисбактериозе и ряде других заболеваний толстой кишки продукция серотонина кишечником значительно снижается.
Массовое высвобождение серотонина из погибающих клеток слизистой желудка и кишечника при воздействии цитотоксических химиопрепаратов является одной из причин возникновения тошноты и рвоты, диареи при химиотерапии злокачественных опухолей. Аналогичное состояние бывает при некоторых злокачественных опухолях, эктопически продуцирующих серотонин.
Большое содержание серотонина также отмечается в матке. Серотонин играет роль в паракринной регуляции сократимости матки и маточных труб и в координацииродов. Продукция серотонина в миометрии возрастает за несколько часов или дней до родов и ещё больше увеличивается непосредственно в процессе родов. Также серотонин вовлечён в процесс овуляции — содержание серотонина (и ряда других биологически активных веществ) в фолликулярной жидкости увеличивается непосредственно перед разрывом фолликула, что, по-видимому, приводит к увеличению внутрифолликулярного давления.
Серотонин оказывает значительное влияние на процессы возбуждения и торможения в системе половых органов. Например, увеличение концентрации серотонина у мужчин задерживает наступление эякуляции.
Химические свойства
Молекула тироксина содержит в себе 4 атома йода. Большая часть тироксина, циркулирующего по крови, связывается стироксинсвязывающим глобулином, период полураспада которого примерно 8 дней.
Выработка тироксина
Тироксин вырабатывается фолликулярными клетками щитовидной железы под контролем тиреотропного гормона (ТТГ). Тироксин имеет свойство накапливаться в ткани щитовидной железы. Этот гормон оказывает более длительное действие, чем многие другие гормоны, поэтому поддержание его постоянного уровня имеет жизненно важное значение для организма. Механизм высвобождения тироксина из щитовидной железы в кровь регулируется его концентрацией в крови. Избыток тироксина подавляет его собственное выделение, тормозя выделение тиреолиберина (ТРГ)гипоталамусом и тиреоидстимулирующиго (ТСГ) гормона аденогипофизом. При снижении в крови уровня тироксина снимается его тормозящее влияние на секрецию ТРГ и ТСГ. Продолжительное охлаждение организма, влияя на центр терморегуляции гипоталамуса, приводит к производству тиреолиберина в гипоталамусе, тиреолиберин действует на аденогипофиз, который вырабатывает тиреоидстимулирующий гормон (ТСГ), а этот гормон действует на щитовидную железу, в которой усиливается синтез и секреция тироксина.
Небольшая часть тироксина циркулирует по крови в свободной форме. В большинстве случаев транспорт тироксина осуществляется в связанном виде.
Тироксин влияет на все ткани организма, для него нет специфичных клеток-мишеней. Этот гормон способен проникать через мембрану и соединяться с рецепторами в каждой клетке организма.
Основной функцией тироксина является активация процессов метаболизма, которая осуществляется через стимуляцию синтеза РНК и соответствующих белков.Тироксин влияет на обмен веществ, повышает температуру тела, контролирует рост и развитие организма, увеличивает синтез белков и чувствительность к катехоламинам, увеличивает частоту сердечных сокращений, утолщает внутреннюю слизистую оболочку матки у женщин. Усиливает окислительные процессы в клетках всего организма, в частности и клетках мозга. Тироксин важен для надлежащего развития и дифференцировки всех клеток человеческого тела, также может стимулировать метаболизм витаминов.
История открытия
Эдвард Ке́лвин Ке́ндалл впервые выделил тироксин из высушенных препаратов щитовидных желез в 1919 году. Шарль Роберт Харингтон охарактеризовал и синтезировал гормон в 1926 году. В том же году Георг Фридрих Хеннинг выпускал препарат тироксин под названием „Thyroxin Henning“ для страдающих заболеваниями щитовидной железы.
Чрезмерная и недостаточная активность щитовидной железы может сопровождаться увеличением ее размеров. При повышенной секреции тироксина развиваетсягипертиреоз. Крайняя степень гипертиреоза называется базедовой болезнью и может привести к сердечной недостаточности. Недостаток гормона или гипотиреоз в раннем возрасте может привести к кретинизму, а в более зрелом возрасте к микседеме.
Применение в медицине
L-тироксин или левотироксин − это синтетический аналог тироксина. Он используется для нормализации работы щитовидной железы при гипотиреозе и базедовой болезни. L-тироксин стимулирует рост и развитие тканей, повышает их потребность в кислороде, стимулирует обмен веществ, повышает работу нервной и сердечно-сосудистой систем. При повышенных дозах L-тироксин угнетает выработку гормонов гипоталамуса (ТРГ) и аденогипофиза (ТСГ). L-тироксин легко поглощается пищеварительной системой.
Адреналин (эпинефрин) (L-1 (3,4-Диоксифенил)-2-метиламиноэтанол) — основной гормон мозгового вещества надпочечников, а также нейромедиатор. По химическому строению является катехоламином. Адреналин содержится в разных органах и тканях, в значительных количествах образуется в хромаффинной ткани, особенно в мозговом веществе надпочечников.
Синтетический адреналин используется в качестве лекарственного средства под наименованием «Эпинефрин» (МНН).
Адреналин вырабатывается нейроэндокринными клетками мозгового вещества надпочечников и участвует в реализации состояния, при котором организм мобилизируется для устранения угрозы. Его секреция резко повышается при стрессовыхсостояниях, пограничных ситуациях, ощущении опасности, при тревоге, страхе, при травмах, ожогах и шоковых состояниях. Содержание адреналина в крови повышается, в том числе, и при усиленной мышечной работе. Действие адреналина связано с влиянием на α- и β-адренорецепторы и во многом совпадает с эффектами возбуждения симпатических нервных волокон. Он вызывает сужение сосудов органов брюшной полости, кожи и слизистых оболочек; в меньшей степени сужает сосуды скелетной мускулатуры, но расширяет сосуды головного мозга. Артериальное давление под действием адреналина повышается. Однако прессорный эффект адреналина выражен менее, чем у норадреналина в связи с возбуждением не только α1 и α2-адренорецепторов, но и β2-адренорецепторов сосудов (см. ниже). Изменения сердечной деятельности носят сложный характер: стимулируя β1 адренорецепторы сердца, адреналин способствует значительному усилению и учащению сердечных сокращений, облегчению атриовентрикулярной проводимости, повышению автоматизма сердечной мышцы, что может привести к возникновению аритмий. Однако из-за повышения артериального давления происходит возбуждение центра блуждающих нервов, оказывающих на сердце тормозящее влияние, может возникнуть преходящая рефлекторная брадикардия. На артериальное давление адреналин оказывает сложное влияние. В его действии выделяют 4 фазы (см схему):
· Сердечная, связанная с возбуждением β1 адренорецепторов и проявляющаяся повышением систолического артериального давления из-за увеличения сердечного выброса;
· Вагусная, связанная со стимуляцией барорецепторов дуги аорты и сонного клубочка повышенным систолическим выбросом. Это приводит к активации дорсального ядра блуждающего нерва и включает барорецепторный депрессорный рефлекс. Фаза характеризуется замедлением частоты сердечных сокращений (рефлекторная брадикардия) и временным прекращением подъёма артериального давления;
· Сосудистая прессорная, при которой периферические вазопрессорные эффекты адреналина «побеждают» вагусную фазу. Фаза связана со стимуляцией α1 и α2 адренорецепторов и проявляется дальнейшим повышением артериального давления. Следует отметить, что адреналин, возбуждая β1 адренорецепторы юкстагломерулярного аппарата нефроновпочек, способствует повышению секреции ренина, активируя ренин-ангиотензин-альдостероновую систему, также ответственную за повышение артериального давления.
· Сосудистая депрессорная, зависящая от возбуждения β2 адренорецепторов сосудов и сопровождающаяся снижением артериального давления. Эти рецепторы дольше всех держат ответ на адреналин.
Фазы действия адреналина на артериальное давление
На гладкие мышцы адреналин оказывает разнонаправленное действие, зависящее от
источник